题目内容
在醋酸溶液中,CH3COOH电离达到平衡的标志是
| A.溶液显电中性 |
| B.溶液中检测不出CH3COOH分子存在 |
| C.氢离子浓度恒定不变 |
| D.c(H+)=c(CH3COO-) |
C
电离平衡为:CH3COOH CH3COO—+H+
CH3COO—+H+
溶液本身就是电中性,排除A;由于醋酸为弱电解质,不可能全部电离,所以溶液中任何时间都能检测出CH3COOH分子,排除B;在电离过程中c(H+)与c(CH3COO-)任何时候都相等,也不能做为平衡标志,排除D;故答案为C:当氢离子浓度不变时,电离达到平衡
 CH3COO—+H+
CH3COO—+H+溶液本身就是电中性,排除A;由于醋酸为弱电解质,不可能全部电离,所以溶液中任何时间都能检测出CH3COOH分子,排除B;在电离过程中c(H+)与c(CH3COO-)任何时候都相等,也不能做为平衡标志,排除D;故答案为C:当氢离子浓度不变时,电离达到平衡

练习册系列答案
相关题目
 2H+ + S2-
2H+ + S2- NH4+ +OH-的平衡,如果使平衡向逆反应方向移动,同时使c(OH-)增大,应加入 ( )
NH4+ +OH-的平衡,如果使平衡向逆反应方向移动,同时使c(OH-)增大,应加入 ( ) 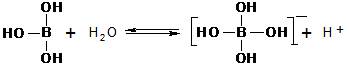
 已知H2A的电离方程式为:H2A ="=" H++HA-; HA- H++A2-。试判断H2A是 电解质(填“强”或“弱”)。
已知H2A的电离方程式为:H2A ="=" H++HA-; HA- H++A2-。试判断H2A是 电解质(填“强”或“弱”)。
 (4)已知CH3COO-+H+ CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是( )
(4)已知CH3COO-+H+ CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是( )