题目内容
现有稀硫酸和稀硝酸的混合溶液,已知其中稀硫酸浓度为4mol/L,稀硝酸的浓度为2mol/L.取10mL混合酸,向其中加入过量铁粉,反应结束后,在标准状况下可收集到气体体积为(假设HNO3只被还原为NO)( )
| A.0.224L | B.0.448L | C.0.672L | D.0.896L |
10mL混合酸中含有:n(H+)=0.01L×2×4mol/L+0.01L×2mol/L=0.1mol,n(NO3-)=0.01L×2mol/L=0.02mol,
由于铁过量,则发生反应:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O,Fe+2H+=Fe2++H2↑,则
3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O
0.02mol 0.08mol 0.02mol
反应后剩余n(H+)=0.1mol-0.08mol=0.02mol,
Fe+2H+=Fe2++H2↑
0.02mol 0.01mol
所以:n(NO)+n(H2)=0.02mol+0.01mol=0.03mol,
V(NO)+V(H2)=0.03mol×22.4L/mol=0.672L,
故选C.
由于铁过量,则发生反应:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O,Fe+2H+=Fe2++H2↑,则
3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O
0.02mol 0.08mol 0.02mol
反应后剩余n(H+)=0.1mol-0.08mol=0.02mol,
Fe+2H+=Fe2++H2↑
0.02mol 0.01mol
所以:n(NO)+n(H2)=0.02mol+0.01mol=0.03mol,
V(NO)+V(H2)=0.03mol×22.4L/mol=0.672L,
故选C.

练习册系列答案
相关题目

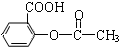 ).为测定某解热镇痛药阿斯
).为测定某解热镇痛药阿斯 冷却后用0.10mol/LHCl溶液返滴过量的NaOH,消耗该HCl溶液25.00mL.
冷却后用0.10mol/LHCl溶液返滴过量的NaOH,消耗该HCl溶液25.00mL.