题目内容
关于原电池的叙述中正确的是( )。
| A.任何化学反应,均可以设计成原电池 |
| B.原电池是把化学能直接转化成电能的装置 |
| C.原电池的两极必须都是金属 |
| D.原电池都可以提供持续稳定的电流,应用十分广泛 |
B
解析

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是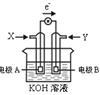
| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
全世界每年钢铁因锈蚀造成大量的损失。某城市拟用如图方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀。关于此方法,下列说法不正确的是
| A.土壤中的钢铁易被腐蚀是因为在潮湿的土壤中形成了原电池 |
| B.金属棒M的材料应该是比镁活泼的金属 |
C.金属棒M上发生反应: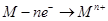 |
| D.这种方法称为牺牲阳极的阴极保护法 |
新型LiFePO4可充电锂离子动力电池以其独特的优势成为绿色能源的新宠。已知该电池放电时的电极反应为:正极:FePO4+Li++e- LiFePO4,负极:Li-e-
LiFePO4,负极:Li-e- Li+。下列说法中正确的是( )
Li+。下列说法中正确的是( )
| A.充电时动力电池上标注“+”的电极应与外接电源的正极相连 |
B.放电时电池反应为FePO4+Li++e- LiFePO4 LiFePO4 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上Li+得电子被还原 |
已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一
定量的烧碱溶液达到沉淀溶解平衡,测得pH=13,则下列说法不正确的是( )
| A.所得溶液中的c(H+)=1.0×10-13 mol·L-1 |
| B.所得溶液中由水电离产生的c(OH-)=1.0×10-13 mol·L-1 |
| C.所加的烧碱溶液的pH=13.0 |
| D.所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1 |
随着人们生活质量的不断提高,废电池进行集中处理的问题被提到议事日程,其首要原因是( )。
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等金属离子对土壤和水源的污染 |
| C.不使电池中渗泄的电解液腐蚀其他的物品 |
| D.回收其中的石墨电极 |
某新型电池,以NaBH4(B的化合价为+3)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是 ( )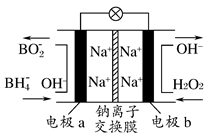
| A.电池工作时Na+从b极区移向a极区 |
| B.每消耗3 mol H2O2,转移3 mol e- |
| C.b极上的电极反应式为:H2O2+2e-+2H+=2H2O |
| D.a极上的电极反应式为:BH4—+8OH--8e-=BO2—+6H2O |
如图中,两电极上发生的电极反应如下:
a极:Cu2++2e-=Cu;b极:Fe-2e-=Fe2+,则以下说法中不正确的是( )。
| A.该装置一定是原电池 |
| B.a极上一定发生还原反应 |
| C.a、b可以是同种电极材料 |
| D.该过程中能量的转换可以是电能转化为化学能 |
