题目内容
【题目】将一定量Fe、FeO 和Fe2O3的混合物加入240mL2mol·L-1稀硝酸中,恰好完全反应,放出1.344L(标准状况下)NO 气体,往所得溶液中加入酸性KMnO4溶液,无明显现象。若用足量的H2在加热条件下与相同质量的上述混合物充分反应,能得到铁的质量为
A.6.72gB.7.84gC.8.96gD.13.4g
【答案】B
【解析】
因一定量的Fe、FeO和Fe2O3的混合物中加入240mL 2molL-1的稀硝酸,恰好使混合物完全溶解,往所得溶液中加入KMnO4的酸性溶液,无明显现象,说明溶液中的溶质为硝酸铁,1.344LNO(标准状况)的物质的量为:![]() =0.06mol,根据氮元素守恒,硝酸铁中的硝酸根离子的物质的量为:0.24L×2mol/L-0.06mol=0.42mol,所以硝酸铁的物质的量为:
=0.06mol,根据氮元素守恒,硝酸铁中的硝酸根离子的物质的量为:0.24L×2mol/L-0.06mol=0.42mol,所以硝酸铁的物质的量为:![]() ×0.42mol=0.14mol,由铁元素守恒可知,得到铁的物质的量为n(Fe)=0.14mol,质量为0.14mol×56g/mol=7.84g,答案选B。
×0.42mol=0.14mol,由铁元素守恒可知,得到铁的物质的量为n(Fe)=0.14mol,质量为0.14mol×56g/mol=7.84g,答案选B。

【题目】已知SO3分解反应为2SO3(g)2SO2(g)+O2(g)。在1.0L密闭容器中加入10mol SO3(g),在一定温度进行上述反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/kPa | 400 | 412 | 422 | 440 | 469 | 518 | 538 | 560 | 560 |
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为_____(填字母)。
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为_____,该温度下的平衡常数Kw=_____
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPamin﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=_____kPa,v(SO3)=_____kPamin﹣1。
【题目】向物质Y中逐渐加入(或通入)X溶液,生成沉淀的量与加入X的物质的量关系如图所示,下表中符合图示情况的是
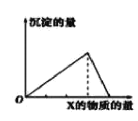
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D