题目内容
5.某厂排放的废水中含有碳酸钠,未经处理,会造成污染.化学兴趣小组的同学对废水处理设计了如图所示的实验方案.试计算:
(1)反应生成CO2气体的质量是2.2g.
(2)反应后所得溶液中溶质的质量分数?
分析 (1)根据反应前后的质量差可以计算生成二氧化碳的质量;
(2)根据二氧化碳的质量可以计算反应生成氯化钠的质量,进一步可以计算反应后所得溶液中溶质的质量分数.
解答 解:(1)反应生成CO2气体的质量为:100g+19.2g-117g=2.2g;
故答案为:2.2;
(2)设生成氯化钠的质量为x,
Na2CO3+2HC1═2NaC1+H2O+CO2↑
117 44
x 2.2g
x=5.85g
反应后所得溶液中溶质的质量分数为:$\frac{5.85g}{117g}$×100%=5%
答:反应后所得溶液中溶质的质量分数为5%.答:反应后所得溶液中溶质的质量分数为5%.
点评 本题考查了溶液质量分数的求算、有关方程式的计算,题目难度不大,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
15.NaCl是一种化工原料,可以制备一系列物质,如图所示.下列说法正确的是( )
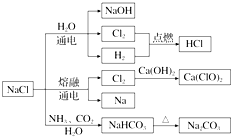

| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的Cl2能用钢瓶贮运,所以Cl2在任何条件下都不与铁反应 | |
| D. | 图示转化反应都是氧化还原反应 |
13.下列溶液中的Cl-的物质的量浓度与100mL 1mol•L-1AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A. | 50mL 3 mol•L-1的KCl溶液 | B. | 150mL 1 mol•L-1的FeCl2溶液 | ||
| C. | 150mL 1 mol•L-1的MgCl2溶液 | D. | 300mL 1 mol•L-1的NaCl溶液 |
20.用下列装置进行的相应实验能达到实验目的是( )

| A. | 图1装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. | 图2装置用于分离水和溴苯的混合物 | |
| C. | 图3装置用于制备并收集NO气体 | |
| D. | 图4装置用于除去碳酸氢钠固体中的少量碳酸钠 |
10.下列离子方程式书写正确的是( )
| A. | 氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+ | |
| B. | 碳酸钠溶于醋酸溶液中:CO32-+2 H+=H2O+CO2↑ | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 硫酸与氢氧化钡溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
17.下列有关物质的性质或应用正确的是( )
| A. | 实验室常用铝盐溶液与氢氧化钠溶液制备Al(OH)3沉淀 | |
| B. | 浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 | |
| C. | SO2 具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
 有A、B、C、D、E、F六种物质,它们的相互转化关系如图(反应条件及部分产物乙略).已知A、B、E均为单质,B、E在常温下为气体,C为淡黄色固体.回答下列问题:
有A、B、C、D、E、F六种物质,它们的相互转化关系如图(反应条件及部分产物乙略).已知A、B、E均为单质,B、E在常温下为气体,C为淡黄色固体.回答下列问题: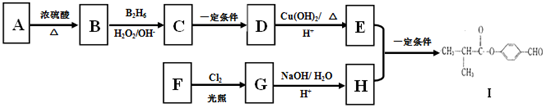
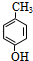 .
.
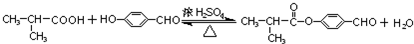
 .
.