题目内容
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡.请根据所学知识的回答:
(1)A为0.1mol/L的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为________________
(2)B为0.1mol/LNaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(用离子方程式表示):____________;___________;__________。
实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:________________
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入________________目的是_____________;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程为_________________.
(4)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25℃时,氯化银的Ksp=1.8×10-10mol2/L2.现将足量氯化银分别放入:
① 100mL蒸馏水中;
② 100mL 0.2mol/LAgNO3溶液中;
③ 100mL 0.1mol/L氯化铝溶液中;
④ 100mL 0.1mol/L盐酸溶液中.充分搅拌后,相同温度下银离子浓度由大到小的顺序_____________(填写序号);②中氯离子的浓度为_________mol/L,③中银离子的浓度为______mol/L
练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目


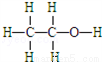 B. 氯原子的结构示意
B. 氯原子的结构示意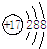
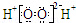 D. 乙烯的最简式:C2H4
D. 乙烯的最简式:C2H4
 2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )
2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )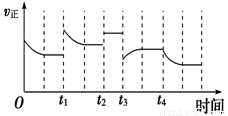
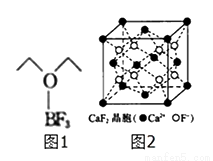
 O2(g) = CO2(g)+2H2O(1) △H1=akJ•mol-1
O2(g) = CO2(g)+2H2O(1) △H1=akJ•mol-1 O2(g) = H2O(1) △H2=bkJ•mol-1
O2(g) = H2O(1) △H2=bkJ•mol-1 CH3OH(g)+H2O(g) △H=__________kJ•mol-1
CH3OH(g)+H2O(g) △H=__________kJ•mol-1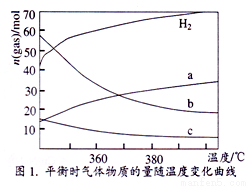
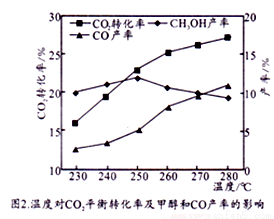
 6FeO+O2↑ ,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
6FeO+O2↑ ,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。