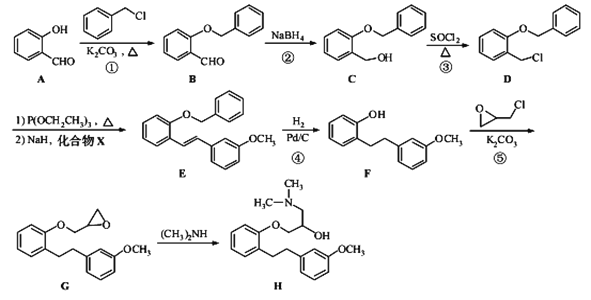
题目内容
【题目】已知铅蓄电池放电时的原电池反应:PbO2+Pb+2H2SO4===2PbSO4+2H2O。关于铅蓄电池的下列说法中正确的是( )
A. 放电时的正极反应式是Pb+SO42--2e-===PbSO4
B. 放电时电池的负极材料是铅板
C. 充电时,电池中硫酸的浓度不断变小
D. 充电时,铅板发生氧化反应
【答案】B
【解析】
根据总反应,放电时,负极的电极反应式为Pb+SO42--2e-═PbSO4,正极的电极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,充电时阴阳极电极反应与负极、正极反应正好相反,据此分析解答。
A.放电时,正极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,故A错误;
B.放电时,Pb被氧化,应为电池的负极,故B正确;
C.该铅蓄电池总反应为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,充电时,生成硫酸,硫酸浓度增大,故C错误;
2PbSO4+2H2O,充电时,生成硫酸,硫酸浓度增大,故C错误;
D.充电时,铅板作阴极,发生还原反应,故D错误;
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】[化学——选修3:物质结构与性质]
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(KJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15399 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背 ,B元素位于周期表五个区域中的 区。
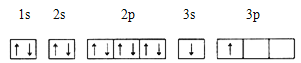
②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①以体心立方堆积形成的金属铁中,其原子的配位数为 。
②写出一种与CN-互为等电子体的单质的电子式 。
③六氰合亚铁离子[Fe(CN)6]4-中不存在 。
A.共价键
B.非极性键
C.配位键
D.σ键
E.π键
(3)一种Al-Fe合金的立体晶胞如右图所示。请据此回答下列问题:
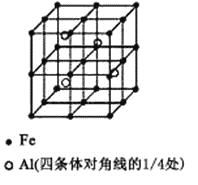
①确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。