题目内容
18.以NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 12g石墨中含有C-C键的个数为3NA | |
| B. | 7.8gNa2O2晶体中含有阴阳离子总数为0.4NA | |
| C. | 1molSiO2晶体中含有2NASi-O键 | |
| D. | 28g乙烯中含π键的数目为NA |
分析 A.在石墨晶体中1个C原子对应3×$\frac{1}{3}$=$\frac{3}{2}$个C-C键;
B.过氧化钠中阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,总共含有0.3mol离子;
C.SiO2晶体中1个Si原子对应4个Si-O键;
D.乙烯分子中含有1个π键,28g乙烯的物质的量为1mol,含有1molπ键.
解答 解:A.在石墨晶体中1个C原子对应3×$\frac{1}{3}$=$\frac{3}{2}$个C-C键,12 g石墨的物质的量为1mol,则12g石墨中含有C-C键的个数为1.5NA,故A错误;
B.7.8g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.2mol钠离子、0.1mol过氧根离子,总共含有0.3mol离子,含有阴阳离子总数为0.3NA,故B错误;
C.SiO2晶体中1个Si原子对应4个Si-O键,1molSiO2中含Si-O键的个数为4NA,故C错误;
D.28g乙烯的物质的量为1mol,1mol乙烯分子中含有1molπ键,含π键的数目为NA,故D正确;
故选D.
点评 本题考查阿佛加德罗常数的综合应用,题目难度中等,明确二氧化硅、石墨中的成键为解答关键,注意熟练掌握物质的量与阿伏伽德罗常数等物理量之间的转化关系.

练习册系列答案
相关题目
8.根据下列操作现象,下属实验目的或结论正确的是( )
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 取1ml20%蔗糖溶液,加入3~5滴稀硫酸,水浴加热5min后,取少量溶液,加入少量新制的Cu(OH)2,加热,没有砖红色沉淀生成 | 蔗糖没有水解 |
| B | SO2通入Ba(NO3)2溶液,生成白色沉淀 | 生成白色Ba(SO3)2沉淀 |
| C | 铜放入稀硫酸中无明显现象,再加入硝酸钠固体,有明显的气泡冒出,溶液变蓝,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向盛有3mL约5%的H2O2溶液中加入1~2滴1mol/LFeCl3溶液;有大量气泡出现,能使带火星的火柴梗复燃 | FeCl3可以催化H2O2分解的反应速率 |
| A. | A | B. | B | C. | C | D. | D |
9.化学能与热能、电能等能相互转化,下列说法正确的是( )

| A. | 图1所示的装置能将化学能转变为电能 | |
| B. | 图2所示的反应为吸热反应 | |
| C. | 化石燃料是可再生能源,燃烧时将化学能转变为热能 | |
| D. | 化学反应中能量变化的主要原因是化学键的断裂与生成 |
6.一瓶失去标签的无色溶液,下列相关说法正确的是( )
| A. | 若溶液是强酸溶液,该溶液中一定含有分子 | |
| B. | 若溶液显碱性,该溶液一定是碱溶液 | |
| C. | 无论是强酸溶液还是强碱溶液,加入金属Al一定会放出H2 | |
| D. | 向该溶液中加入酸化的BaCl2溶液,可验证是否含有SO42- |
13.下列各组原子,彼此性质一定相似的是( )
| A. | 外围电子分别是1s2与2s2的元素 | |
| B. | M层上有两个电子与N层上有两个电子的元素 | |
| C. | 2p上有一个未成对电子与3p上有一个未成对电子的元素 | |
| D. | L层上有一个空轨道和M层的p轨道上有一个空轨道的元素 |
3.W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
( )
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | 简单阴离子还原性X大于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
10.下列物质互为同分异构体的是( )
| A. | 氧气和臭氧 | B. | 正丁烷和异丁烷 | C. | 甲烷和乙烯 | D. | 1H和2H |
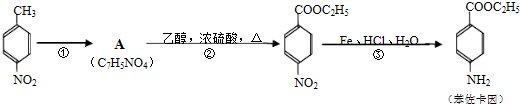
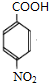 +CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$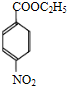 +H2O;
+H2O;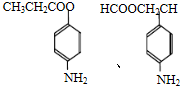 ,则剩余三种同分异构体的结构简式为:
,则剩余三种同分异构体的结构简式为: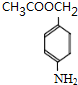 、
、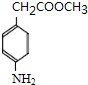 、
、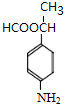 .
.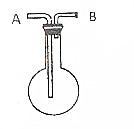 利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)
利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)