题目内容
【题目】100g碳燃烧所得气体中,CO占![]() ,CO2占
,CO2占![]() 体积,且C(s)+
体积,且C(s)+![]() O2(g)===CO(g);ΔH(298K)=-110.35kJ·mol-1,CO(g)+
O2(g)===CO(g);ΔH(298K)=-110.35kJ·mol-1,CO(g)+![]() O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1。与这些碳完全燃烧相比较,损失的热量是( )
O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1。与这些碳完全燃烧相比较,损失的热量是( )
A.392.92kJ B.2489.44kJ
C.784.92kJ D.3274.3kJ
【答案】C
【解析】100g碳不完全燃烧时产生CO物质的量为![]() ×
×![]() mol,因为碳完全燃烧可分两步,先生成CO同时放热,CO再生成CO2再放热,总热量即为完全燃烧时放出的热。因此与100g碳完全燃烧相比,损失的热量为即
mol,因为碳完全燃烧可分两步,先生成CO同时放热,CO再生成CO2再放热,总热量即为完全燃烧时放出的热。因此与100g碳完全燃烧相比,损失的热量为即![]() ×
×![]() mol CO燃烧放出的热量,设为Q。
mol CO燃烧放出的热量,设为Q。
CO(g)+![]() O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1
O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1
1mol 282.57kJ
![]() ×
×![]() mol Q
mol Q
Q=282.57kJ×![]() ×
×![]() mol,Q=784.92kJ。
mol,Q=784.92kJ。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】硫及其化合物对人类的生产和生活有着重要的作用.
2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2 , 反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是 , 判断的依据 . 
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)SO3(g)+NO(g)△H=﹣42kJmol﹣1 .
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= , 该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,TlT2(填“>”“<’’或“=”),判断的理由是 .
【题目】车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
物质 | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(1)写出NO与活性炭反应的化学方程式;
(2)计算上述反应T1℃时的平衡常数K1=;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为;
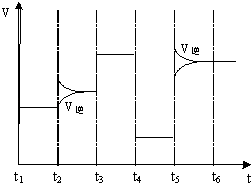
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3﹣t4阶段为使用催化剂.请判断该反应△H0(填“>”或“<”).