题目内容
下列关于反应能量的说法正确的是
| A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)△H=" -216" KJ/mol,反应物总能量小于生成物总能量 |
| B.相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子所具有的能量为E2,则2E2=E1 |
| C.101KPa时,2H2(g)+O2(g) =2H2O(l) △H=" -517.6" KJ/mol,若生成气态水,△H小于-517.6 KJ/mol |
| D.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
D
A.反应放热,说明反应物总能量大于生成物总能量,A错误。
B.1mol氢分子含有2mol氢原子,故其具有的能量为2mol氢原子的总能量,E2=2E1,B错误。
C.液态水转化为气态水要吸热,故生成气态水放出的热量要少,但△H要大,C错误。
D.利用太阳能等清洁能源代替化石燃料,利于节约资源、保护环境,正确。
故选D
B.1mol氢分子含有2mol氢原子,故其具有的能量为2mol氢原子的总能量,E2=2E1,B错误。
C.液态水转化为气态水要吸热,故生成气态水放出的热量要少,但△H要大,C错误。
D.利用太阳能等清洁能源代替化石燃料,利于节约资源、保护环境,正确。
故选D

练习册系列答案
相关题目
 g)="2CO(g)" △H="-221.0" kJ/mol
g)="2CO(g)" △H="-221.0" kJ/mol


 :CO+O2—―2e-=CO2
:CO+O2—―2e-=CO2 时电子由电极a通过传感器流向电极b
时电子由电极a通过传感器流向电极b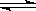 2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是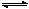 2HI(g)的说法,不正确的是 ( )
2HI(g)的说法,不正确的是 ( )