题目内容
【题目】锌焙砂主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物。下图是工业上利用锌焙砂制取金属锌的流程图。
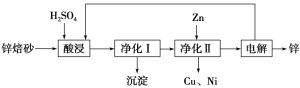
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为_____________________________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式: _________________________________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=________ mol·L-1(已知25 ℃,Ksp[Fe(OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是__________________________________。
(3)本流程中可以循环利用的物质除硫酸锌外还有__________________。
(4)若没有净化Ⅱ操作,则对锌的制备带来的影响是__________________________。
【答案】(1)ZnFe2O4+4H2SO4===ZnSO4+Fe2(SO4)3+4H2O (2)①H2O2+2Fe2++2H+===2Fe3++2H2O ②4.0×10-5 ③Fe(OH)3胶体具有吸附性
(3)H2SO4、Zn (4)制取的锌含铜、镍等杂质
【解析】(1)根据信息,酸浸时ZnFe2O4会生成两种盐,这两种盐分别为硫酸锌、硫酸铁,即ZnFe2O4与硫酸反应的化学方程式为ZnFe2O4+4H2SO4===ZnSO4+Fe2(SO4)3+4H2O。(2)①亚铁离子被双氧水氧化成铁离子,反应的离子方程式为H2O2+2Fe2++2H+===2Fe3++2H2O;②氢氧化铁的溶度积Ksp[Fe(OH)3]=4.0×10-38,pH=3的溶液中,氢氧根离子的浓度为1×10-11 mol·L-1,c(Fe3+)=![]() mol·L-1=4.0×10-5 mol·L-1。(3)通过制取金属锌的流程图可知,可以循环利用的物质除硫酸锌外,还有硫酸、锌。(4)由于锌焙砂中含有CaO、FeO、CuO、NiO等氧化物,酸浸后溶液中存在钙离子、亚铁离子、铜离子、镍离子,如果没有净化Ⅱ操作,则电解制取的锌中会含有铜、镍等杂质。
mol·L-1=4.0×10-5 mol·L-1。(3)通过制取金属锌的流程图可知,可以循环利用的物质除硫酸锌外,还有硫酸、锌。(4)由于锌焙砂中含有CaO、FeO、CuO、NiO等氧化物,酸浸后溶液中存在钙离子、亚铁离子、铜离子、镍离子,如果没有净化Ⅱ操作,则电解制取的锌中会含有铜、镍等杂质。

 阅读快车系列答案
阅读快车系列答案