题目内容
【题目】在铜、锌、稀硫酸构成的原电池中(如图所示)。
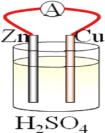
(1)负极是__(填“铜”或“锌”),__电子(填“失去”或“得到”),发生__反应(填“氧化”或“还原”),电极反应方程式___;正极是__(填“铜”或“锌”)__电子(填“失去”或“得到”),发生__反应(填“氧化”或“还原”),电极反应方程式__。
(2)电流由___流向___(填“铜”或“锌),铜片上观察到的现象是___。
【答案】锌 失去 氧化 Zn-2e-=Zn2+ 铜 得到 还原 2H++2e-=H2↑ 铜 锌 有气泡产生
【解析】
(1)金属性锌强于铜,因此负极是锌,失去电子,发生氧化反应,电极反应方程式为Zn-2e-=Zn2+;正极是铜得到电子,发生还原反应,电极反应方程式为2H++2e-=H2↑。
(2)电流由正极流向负极,即由铜流向锌,铜片上氢离子放电,观察到的现象是有气泡产生。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D