题目内容
(4分)有一无色透明溶液,可能含Cu2+、NH、Al3+、Fe3+、Mg2+、Na+、K+、CO、SO、NO等离子中的若干种。现做如下实验:
①取少量该溶液,滴入用盐酸酸化的BaCl2溶液,有白色沉淀生成。
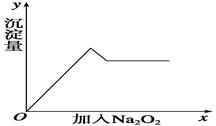
②另取部分溶液,加入过氧化钠,有无色气体放出,且有白色沉淀产生,加入过氧化钠的量与生成白色沉淀的量可用右图表示。
试推断:
(1)该溶液中一定存在__________________,一定不存在____________________,可能存在______________。
(2)上述溶液中至少有______________________等物质混合而成。
①取少量该溶液,滴入用盐酸酸化的BaCl2溶液,有白色沉淀生成。
②另取部分溶液,加入过氧化钠,有无色气体放出,且有白色沉淀产生,加入过氧化钠的量与生成白色沉淀的量可用右图表示。

试推断:
(1)该溶液中一定存在__________________,一定不存在____________________,可能存在______________。
(2)上述溶液中至少有______________________等物质混合而成。
(1)Al3+、Mg2+、SO; Cu2+、NH、Fe3+、CO; Na+、K+、NO
(2)Al2(SO4)3、MgSO4
(2)Al2(SO4)3、MgSO4
试题分析:(1)因是“无色透明溶液”,该溶液中不能含有有色离子 Cu2+、Fe3+.根据①的信息,说明溶液中含有 SO42-,没有 CO32- (与盐酸反应生成二氧化碳).向溶液中加入过氧化钠,产生无色无味气体,说明该溶液中不含 NH4+,因为若有 NH4+,会与过氧化钠与水反应生成的氢氧化钠反应生成氨气,氨气具有刺激性气味.当向溶液中加入过氧化钠时,会生成白色沉淀,且沉淀量先增加后减少,但不会完全消失,说明溶液中含有Al3+、Mg2+,因为它们分别能与氢氧化钠反应生成氢氧化铝沉淀和氢氧化镁沉淀,而氢氧化铝能继续与过量氢氧化钠反应生成偏铝酸钠而使沉淀减少.因此,该溶液中一定存在的离子有:Al3+、Mg2+、SO.
当溶液中含有Al3+、Mg2+、SO时,既存在阴离子又存在阳离子,因此Na+和K+可能存在,也可能不存在.
因是“无色透明溶液”,该溶液中不能含有有色离子 Cu2+、Fe3+,因此,一定不存在的离子有:Cu2+、Fe3+、CO32-、NH4+.
故答案为:Al3+、Mg2+、SO; Cu2+、NH、Fe3+、CO; Na+、K+、NO
(2)、溶液中含有的溶质应电离出一定含有的离子,故为Al2(SO4)3、MgSO4
点评:本题把离子之间的反应与图象结合起来,增大了题目的难度,因此要把所学知识与图象结合起来.另外,由于部分同学没注意到“无色透明溶液”而不能做出正确判断,说明一定要加强审题训练.

练习册系列答案
相关题目
 的硫化钾溶液中:
的硫化钾溶液中:

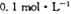 的NH4Cl溶液中:
的NH4Cl溶液中: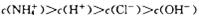
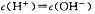
 Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 )>c(H+)
)>c(H+)