题目内容
HClO是比碳酸还弱的酸,反应:Cl2+H2O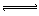 HCl+HClO达平衡后,要使HClO浓度增加,可加入
HCl+HClO达平衡后,要使HClO浓度增加,可加入
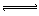 HCl+HClO达平衡后,要使HClO浓度增加,可加入
HCl+HClO达平衡后,要使HClO浓度增加,可加入 | A.H2S(气) |
| B.HCl |
| C.CaCO3(固) |
| D.H2O |
C
本题要求所加入的物质可破坏原化学平衡并增大[HClO]的浓度。
A项通入的为H2S气体是还原剂,而HClO具有氧化性,所以H2S一定会和HClO反应,故A不是答案。加入盐酸平衡向逆方向移动,也会减少HClO,故B也不是答案。加入CaCO3后CaCO3可与HCl反应,但不与HClO反应。因为三种酸的酸性由强至弱的顺序是HCl>H2CO3>HClO,所以盐酸能和碳酸钙反应,而HClO的酸性比H2CO3弱,所以不能与CaCO3反应,加入CaCO3可减小HCl浓度平衡向正方向移动而HClO不参加反应,其浓度增大。C为答案。加入水后,化学平衡虽能向正反应方向移动。但加水后溶液冲稀,HClO浓度也减小。
A项通入的为H2S气体是还原剂,而HClO具有氧化性,所以H2S一定会和HClO反应,故A不是答案。加入盐酸平衡向逆方向移动,也会减少HClO,故B也不是答案。加入CaCO3后CaCO3可与HCl反应,但不与HClO反应。因为三种酸的酸性由强至弱的顺序是HCl>H2CO3>HClO,所以盐酸能和碳酸钙反应,而HClO的酸性比H2CO3弱,所以不能与CaCO3反应,加入CaCO3可减小HCl浓度平衡向正方向移动而HClO不参加反应,其浓度增大。C为答案。加入水后,化学平衡虽能向正反应方向移动。但加水后溶液冲稀,HClO浓度也减小。

练习册系列答案
相关题目
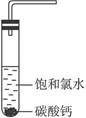
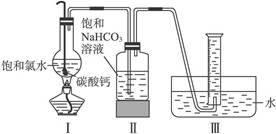
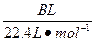 明显小于
明显小于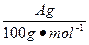 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。