题目内容
水的电离平衡曲线如图所示,下列说法不正确的是 ( )
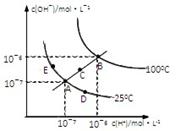
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:保持温度不变, 在水中加入少量的酸
C.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
D.若从A点到C点,可采用:在水中加入适量的NH4NO3固体的变化
【答案】
D
【解析】
试题分析:水的电离是吸热的,则温度高,水的离子积常数大,所以根据图像可知图中五点KW间的关系:B>C>A=D=E,A正确;从A点到D点,溶液中氢离子的浓度增大,但温度不变,所以选项B正确;处在B点时,pH=2的硫酸中氢离子浓度是0.01mol/L,pH=10的KOH中OH-的浓度是0.01mol/L,则等体积混合后,溶液显中性,C正确;从A点到C点,温度升高,所以选项D不正确,答案选D。
考点:考查水的离子积常数常数的判断、应用以及溶液酸碱性的判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,综合性强,在注重对学生基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确温度对离子积常数的影响,然后灵活运用即可。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示. (2006?成都模拟)水的电离平衡曲线如图所示:
(2006?成都模拟)水的电离平衡曲线如图所示: (2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)=
(2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)= (2011?烟台模拟)水的电离平衡曲线如图所示:
(2011?烟台模拟)水的电离平衡曲线如图所示: