题目内容
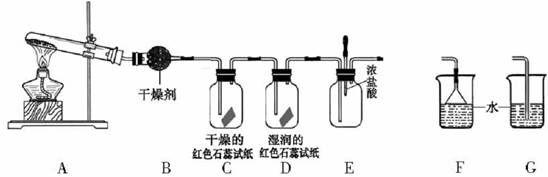
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质.
(1)A中的化学反应方程式是
(2)B中的干燥剂是
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到的现象是
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
分析:(1)实验室制备氨气的原理是氯化铵和氢氧化钙固体在加热条件下反应;
(2)氨气是一种能够碱性气体,应选择碱性干燥剂;
(3)氨气极易和氯化氢气体反应生成氯化铵固体颗粒;
(4)氨气极易溶于水,注意吸收氨气时应防倒吸.
(2)氨气是一种能够碱性气体,应选择碱性干燥剂;
(3)氨气极易和氯化氢气体反应生成氯化铵固体颗粒;
(4)氨气极易溶于水,注意吸收氨气时应防倒吸.
解答:解:(1)实验室制备氨气的原理:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)碱石灰是一种碱性干燥剂,可以用来干燥氨气,故答案为:碱石灰;
(3)氨气极易和氯化氢气体反应:NH3+HCl=NH4Cl,生成固体颗粒氯化铵,现象是:产生大量白烟,故答案为:产生大量白烟;
(4)F装置能防止发生倒吸,G装置容易发生倒吸,故答案为:F.
| ||
| ||
(2)碱石灰是一种碱性干燥剂,可以用来干燥氨气,故答案为:碱石灰;
(3)氨气极易和氯化氢气体反应:NH3+HCl=NH4Cl,生成固体颗粒氯化铵,现象是:产生大量白烟,故答案为:产生大量白烟;
(4)F装置能防止发生倒吸,G装置容易发生倒吸,故答案为:F.
点评:本题考查了氨气的实验室制法,题目简单,结合氨气的性质不难找到答案.

练习册系列答案
相关题目



 CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O