题目内容
等体积、pH相同的氨水与NaOH溶液,下列说法正确的是
| A.分别加水稀释相同的倍数,稀释后两溶液pH仍相同 |
| B.NaOH溶液中水电离产生的c(OH-)较小 |
| C.用等浓度的盐酸完全中和,消耗盐酸体积相等 |
| D.加入少量NH4Cl(s),pH均减小 |
D
解析试题分析:A、因为加水稀释能促进弱碱的电离平衡向右移动,所以分别加水稀释相同的倍数,稀释后两溶液pH:氨水 > NaOH,错误;B、因为氨水和NaOH溶液的pH相同,即碱电离出的OH?浓度相同,所以对水的电离平衡的抑制作用也相同,水电离产生的OH?离子浓度相同,错误;C、氨水的电离程度小,则氨水的浓度远远大于NaOH浓度,所以用等浓度的盐酸完全中和,氨水消耗盐酸体积多,错误;D、加入少量NH4Cl(s),抑制氨水的电离平衡,NH4Cl能与NaOH反应生成弱碱,所以pH均减小,正确。
考点:本题考查强弱电解质。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述不正确的是
| A.在稀盐酸中c(H+)=c(Cl-)+c(OH-) |
| B.常温下,在0.1mol/L的硫酸铵溶液中由水电离出的c(OH-)>10-7mol/L |
| C.如果Na2A的水溶液显中性,该溶液中一定没有电离平衡 |
| D.热水中加入硫酸钠溶解至饱和,此时溶液的pH小于7 |
常温时,下列叙述正确的是 ( )
| A.稀释pH=3的醋酸,溶液中所有离子的浓度均降低 |
B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,则混合液中 |
| C.pH均为11的NaOH和Na2CO3溶液中,水的电离程度相同 |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
下列叙述中一定正确的是
| A.任何浓度溶液的酸碱性都可用pH试纸测定 |
| B.某温度下,pH=6.2的纯水显酸性 |
| C.25℃时,pH=1的醋酸溶液中c(H+)是pH=2的盐酸溶液中c(H+)的10倍 |
| D.25℃时,pH=12的NaOH溶液中的n(OH-)=10-2mol |
水是一种极弱的电解质,在室温下,KW=1×10-14,则此时水的电离百分数为:
| A.1×10-7 | B.1/55.6 | C.10-14 | D.1/(55.6×107) |
已知Ksp(AgCl) =1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12 。在只含有KCl、K2CrO4的混合溶液中滴加0.001000 mol/L的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×l0-3 mo l/L,此时溶液中Cl-的物质的量浓度是
| A.8. 90×10-6 mol/L | B.1. 36×10-5 mol/L |
| C.1×10-5mol/L | D.4. 45×10-2mol/L |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A.pH=4的醋酸中:c(H+)=4.0 mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)=c(HCO3—) |
| C.饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1 |
下列说法正确的是( )。
A.0.1 mol·L-1的醋酸溶液加水稀释, 减小 减小 |
| B.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
| D.常温下,V1 L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )。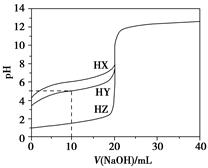
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
| B.根据滴定曲线,可得Ka(HY)≈10-5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) |
D.HY与HZ混合,达到平衡时c(H+)= +c(Z-)+c(OH-) +c(Z-)+c(OH-) |