题目内容
【题目】(1)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:________________________。
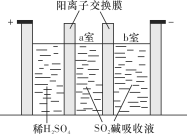
(2)制备焦亚硫酸钠Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为____________。电解后,__________室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。
(3)利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为____________________。(离子交换膜只允许OH-通过)
 .
.
【答案】HNO2-2e-+H2O===3H++NO3- 2H2O-4e-===4H++O2↑ a 2Cu-2e-+2OH-===Cu2O+H2O
【解析】
(1)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸,说明电解时阳极上亚硝酸根离子失电子生成硝酸根离子,其电极反应式为HNO2-2e-+H2O=3H++NO3-,故答案为:HNO2-2e-+H2O=3H++NO3-;
(2)电解池阳极室为稀硫酸溶液,电解质溶液显酸性,电解池阳极发生氧化反应,所以应为H2O放电,产生O2和H+,则电极反应为:2H2O-4e-═O2↑+4H+,溶液中分隔各个室的膜为阳离子交换膜,阳离子向阴极移动,H+向右移动,在b室则发生反应:2H++2e-═H2↑,所以b室较a室H+浓度有所降低,因此电解后,a室的NaHSO3浓度增加,故答案为:2H2O-4e-═O2↑+4H+;a;
(3)利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O。在电解池中,铜当阳极,铜是活泼电极,电极本身发生失去电子的氧化反应,在碱性环境下,电极反应为2Cu-2e-+2OH-=Cu2O+H2O,故答案为:2Cu-2e-+2OH-=Cu2O+H2O。

【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为__________反应(“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。