题目内容
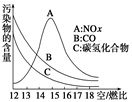
稀薄燃烧是指汽油在较大空气/燃比(空气与燃油气的体积比)条件
下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的
重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为
N2。不同空/燃比时汽车尾气中主要污染物的含量变化如图所示。
(1)稀薄燃烧技术除能节约能源外,还具有的优点是 (填一项)。排放到大气中的NOx会导致酸雨、 等环境问题(填一项)。
(2)某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。
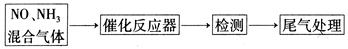







若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通入滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,
需要测量并记录的数据是 。
(3)若某一催化剂能同时催化NH3等还原性气体与NOx的反应。将该催化剂分别用于催化还原含等物质的量NOx的两种气体:①纯NO气体,②汽车尾气。消耗NH3的物质的量较多的可能是 (填字母),原因是 。
A.① B.② C.都有可能
(1)减少CO和碳氢化合物的污染 光化学烟雾或破坏臭氧层
(2)溶液显色所需要的时间
(3)A 汽车尾气中含有一定量的CO和碳氢化合物,少消耗NH3或B 汽车尾气中含有一定量的NO2,多消耗NH3或C 汽车尾气中同时含有CO、碳氢化合物等还原性气体和NO2等氧化性气体,二者相对含量的不同可导致消耗NH3的增多或减少
解析:
(2)溶液显色所需要的时间
(3)A 汽车尾气中含有一定量的CO和碳氢化合物,少消耗NH3或B 汽车尾气中含有一定量的NO2,多消耗NH3或C 汽车尾气中同时含有CO、碳氢化合物等还原性气体和NO2等氧化性气体,二者相对含量的不同可导致消耗NH3的增多或减少
解析:
本题以燃油气燃烧过程产生污染这一社会关注问题为背景,考查了环保知识和探究催化剂性能的过程及问题分析,这是一道开放性、探究性很好的试题,侧重考查了学生的自学能力、分析探究问题的能力,要求学生平日要善于思考和分析,关注社会热点,善于运用所学知识解释和解决生活中遇到的实际问题、做到理论联系实际。
(1)因燃油气燃烧过程中可产生对空气有污染的CO、NOx、碳氢化合物等大气污染物,结合“空/燃比”的含义和题图可以推知,增大“空/燃比”可以减少CO、碳氢化合物的排放从而减少污染,根据课本知识可推出排放到大气中的NOx可导致酸雨及光化学烟雾(或破坏臭氧层)而引起环境污染。
(2)因实验的目的是探究催化剂的催化性,而从所给的探究步骤中,有滴有酚酞的稀硫酸(该溶液为无色),所以肯定是利用NH3与硫酸的酚酞溶液作用显红色的快慢来检测催化性能。只要记录显色所需时间即可。
(3)根据氧化还原反应中电子得失守恒原则可推知,若汽车尾气中会有一定量的CO和碳氢化合物,因它们也可以还原NOx,则所消耗氨气就少,若汽车尾气中含NO2,则因NO2也可氧化NH3,则消耗的氨气就多。
(1)因燃油气燃烧过程中可产生对空气有污染的CO、NOx、碳氢化合物等大气污染物,结合“空/燃比”的含义和题图可以推知,增大“空/燃比”可以减少CO、碳氢化合物的排放从而减少污染,根据课本知识可推出排放到大气中的NOx可导致酸雨及光化学烟雾(或破坏臭氧层)而引起环境污染。
(2)因实验的目的是探究催化剂的催化性,而从所给的探究步骤中,有滴有酚酞的稀硫酸(该溶液为无色),所以肯定是利用NH3与硫酸的酚酞溶液作用显红色的快慢来检测催化性能。只要记录显色所需时间即可。
(3)根据氧化还原反应中电子得失守恒原则可推知,若汽车尾气中会有一定量的CO和碳氢化合物,因它们也可以还原NOx,则所消耗氨气就少,若汽车尾气中含NO2,则因NO2也可氧化NH3,则消耗的氨气就多。

练习册系列答案
相关题目