题目内容
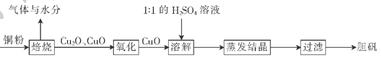
(14分)医用氯化钙 可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为:
可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为:
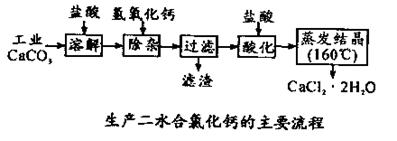
(1)CaCO3与盐酸反应的离子方程式 。
(2)过滤时需用的玻璃仪器除烧杯、玻璃棒外还有 。滤渣主要成分的化学式 。
(3)酸化时加盐酸的目的为:
① ,
②防止Ca2+ 在蒸发时发生水解。
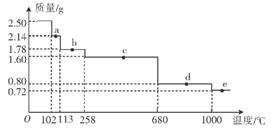
(4)为什么蒸发 结晶要保持在160℃: 。
结晶要保持在160℃: 。
(5)为测定样品中CaCl2 ·2H2O的含量,称取0.7522g样品并配成250mL溶液,分别取该溶液25.00mL于三个锥形瓶中,用0.04mol/LAgNO3溶液进行三次滴定,消耗 AgNO3溶液的平均体积为20.39mL。
①通过计算,样品中含CaCl2 ·2H2O的质量分数 。
②若所测样品 CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为 。
。
 可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为:
可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为: 
(1)CaCO3与盐酸反应的离子方程式 。
(2)过滤时需用的玻璃仪器除烧杯、玻璃棒外还有 。滤渣主要成分的化学式 。
(3)酸化时加盐酸的目的为:
① ,

②防止Ca2+ 在蒸发时发生水解。
(4)为什么蒸发
 结晶要保持在160℃: 。
结晶要保持在160℃: 。(5)为测定样品中CaCl2 ·2H2O的含量,称取0.7522g样品并配成250mL溶液,分别取该溶液25.00mL于三个锥形瓶中,用0.04mol/LAgNO3溶液进行三次滴定,消耗 AgNO3溶液的平均体积为20.39mL。
①通过计算,样品中含CaCl2 ·2H2O的质量分数 。
②若所测样品 CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为
 。
。14分)
(1) CaCO3+ 2H+ ==Ca2+ + CO2↑+ H2O (2分)
(2 ) 普通漏斗(2分) ,Fe(OH)3、 Al(OH)3(2分)
) 普通漏斗(2分) ,Fe(OH)3、 Al(OH)3(2分)
(3)除去过量的氢氧化钙(2分,合理则给分);
(4)温度太高CaCl2 ·2H2O会失水(2分)
(5)(2×147×20.39×10-4/0.7522 )×100%(2分) ==79.69%, Na+没除去析出NaCl,导致测定结果偏(2分)
(1) CaCO3+ 2H+ ==Ca2+ + CO2↑+ H2O (2分)
(2
 ) 普通漏斗(2分) ,Fe(OH)3、 Al(OH)3(2分)
) 普通漏斗(2分) ,Fe(OH)3、 Al(OH)3(2分)(3)除去过量的氢氧化钙(2分,合理则给分);
(4)温度太高CaCl2 ·2H2O会失水(2分)
(5)(2×147×20.39×10-4/0.7522 )×100%(2分) ==79.69%, Na+没除去析出NaCl,导致测定结果偏(2分)
略

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目

 出行
出行