题目内容
 某研究性学习小组通过查阅资料发现,CuSO4溶液与NaOH溶液反应生成的沉淀中除Cu(OH)2外,还有碱式硫酸铜[化学式可表示为xCuSO4?yCu(OH)2].为了加以验证,小组成员进行了如下实验:
某研究性学习小组通过查阅资料发现,CuSO4溶液与NaOH溶液反应生成的沉淀中除Cu(OH)2外,还有碱式硫酸铜[化学式可表示为xCuSO4?yCu(OH)2].为了加以验证,小组成员进行了如下实验:①分别配制50mL物质的量浓度均为0.100mol?L-1CuSO4溶液和NaOH溶液;
②准确量取10mLCuSO4溶液倒入50mL烧杯中;
③向烧杯中匀速加入0.100mol?L-1NaOH溶液,并每加入1.00mLNaOH溶液用pH计测一次混合溶液的pH;
④当滴入NaOH溶液的体积达到30mL时停止实验,并绘制出向CuSO4溶液中滴加NaOH溶液时pH变化曲线.
请回答以下问题:
(1)V(NaOH)在0.00mL~2.00mL之间时,溶液中无沉淀产生,但pH变化较快的原因是
OH-未与Cu2+结合,而是与Cu2+水解产生的H+反应
OH-未与Cu2+结合,而是与Cu2+水解产生的H+反应
;(2)V(NaOH)在2.00mL~15.00mL之间时,溶液中产生绿色沉淀,并不断增加,经检测此沉淀为碱式硫酸铜.已知蒸馏水的pH为6.32,当V(NaOH)为15.00mL时,溶液pH为6.30,则可求得x=
1
1
,y=
2
2
;(3)V(NaOH)在17.00mL~20.00mL之间时,溶液中出现蓝色沉淀,并不断增加.已知V(NaOH)为20.00mL时,溶液pH为12.25,则此时沉淀中
含
含
(填“含”或“不含”)有碱式硫酸铜,理由是加入CuSO4的与NaOH的物质的量之比为1:2,且溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜
加入CuSO4的与NaOH的物质的量之比为1:2,且溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜
.分析:(1)硫酸铜为强酸弱碱盐,水解呈酸性;
(2)当V(NaOH)为15.00mL时,溶液pH为6.30,与蒸馏水的pH相接近,说明加入的NaOH全部生成沉淀,结合质量守恒可确定分子式;
(3)溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜.
(2)当V(NaOH)为15.00mL时,溶液pH为6.30,与蒸馏水的pH相接近,说明加入的NaOH全部生成沉淀,结合质量守恒可确定分子式;
(3)溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜.
解答:解:(1)硫酸铜为强酸弱碱盐,Cu2+水解呈酸性,加入少量NaOH时,OH-未与Cu2+结合,而是与Cu2+水解产生的H+反应,导致溶液中无沉淀产生,但pH变化较快,
故答案为:OH-未与Cu2+结合,而是与Cu2+水解产生的H+反应;
(2)当V(NaOH)为15.00mL时,溶液pH为6.30,与蒸馏水的pH相接近,说明加入的NaOH全部生成沉淀,此时n(Cu2+)=0.01L×0.100mol?L-1=0.001mol,
n(OH-)=0.015L×0.100mol?L-1=0.0015mol,
则有(x+y):2y=0.001mol:0.0015mol=2:3,
则x=1,y=2,
故答案为:1;2;
(3)V(NaOH)为20.00mL时,溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜,
故答案为:含;加入CuSO4的与NaOH的物质的量之比为1:2,且溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜.
故答案为:OH-未与Cu2+结合,而是与Cu2+水解产生的H+反应;
(2)当V(NaOH)为15.00mL时,溶液pH为6.30,与蒸馏水的pH相接近,说明加入的NaOH全部生成沉淀,此时n(Cu2+)=0.01L×0.100mol?L-1=0.001mol,
n(OH-)=0.015L×0.100mol?L-1=0.0015mol,
则有(x+y):2y=0.001mol:0.0015mol=2:3,
则x=1,y=2,
故答案为:1;2;
(3)V(NaOH)为20.00mL时,溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜,
故答案为:含;加入CuSO4的与NaOH的物质的量之比为1:2,且溶液pH为12.25,说明NaOH为完全反应,应存在碱式碳酸铜.
点评:本题考查较为综合,侧重于学生分析能力和计算能力的考查,注意分析图象曲线的变化特点,结合物质的量与物质的性质解答该题,题目难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
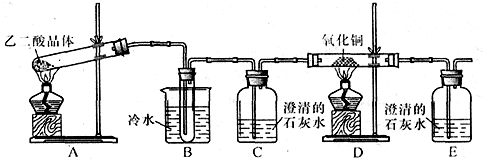
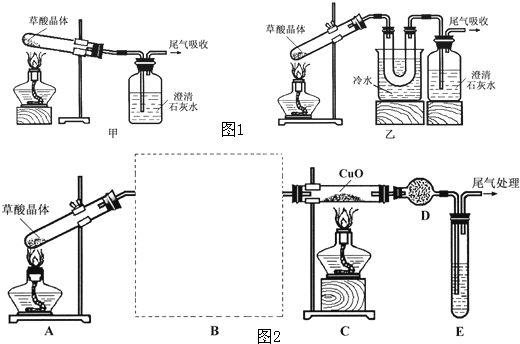
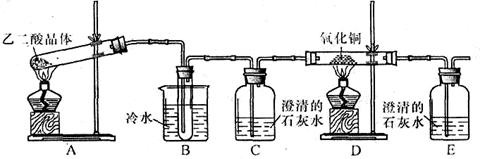
 查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。 进一步探究:
进一步探究: