题目内容
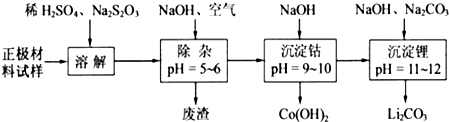
废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴、锂.

(1)在上述溶解过程中,S2O32ˉ被氧化成SO42ˉ,LiCoO2在溶解过程中反应的离子方程式为
(2)除杂时通入空气的目的
(3)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如图乙.
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3.
①a中,阴极的电极反应式是
②b中,生成Li2CO3反应的化学方程式是

(1)在上述溶解过程中,S2O32ˉ被氧化成SO42ˉ,LiCoO2在溶解过程中反应的离子方程式为
S2O32ˉ+8LiCoO2+22H+═2SO42ˉ+8Li++8Co2++11H2O
S2O32ˉ+8LiCoO2+22H+═2SO42ˉ+8Li++8Co2++11H2O
.| 沉淀物 | 开始沉淀pH | 沉淀完全pH |
| Al(OH)3 | 3.0 | 5.2 |
| Fe(OH)3 | 1.5 | 2.8 |
| Fe(OH)2 | 7.6 | 9.7 |
将Fe2+氧化成Fe3+
将Fe2+氧化成Fe3+
,所得的废渣成分为Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
.从废渣中获得Al2O3的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
,步骤Ⅱ中反应的离子方程式是2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ
2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ
.AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ
(3)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如图乙.
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3.
①a中,阴极的电极反应式是
2H++2e-═H2↑或2H2O+2e-═H2+2OH-
2H++2e-═H2↑或2H2O+2e-═H2+2OH-
.②b中,生成Li2CO3反应的化学方程式是
2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3
2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3
.分析:(1)酸性条件下,S2O32ˉ被氧化成SO42ˉ,则LiCoO2被氧化生成Co2+,根据离子方程式的书写规则,再根据氧化还原反应中得失电子结合原子守恒配平方程式;
(2)亚铁离子不稳定易被氧化生成铁离子,根据沉淀所需溶液的pH确定废渣的成分,过滤过程中需要的玻璃仪器是烧杯、漏斗、玻璃棒,偏铝酸盐能和二氧化碳反应生成氢氧化铝沉淀;
(3)①a中,阴极上氢离子放电生成氢气;
②b中,氢氧化锂和碳酸氢铵反应生成碳酸锂和碳酸铵.
(2)亚铁离子不稳定易被氧化生成铁离子,根据沉淀所需溶液的pH确定废渣的成分,过滤过程中需要的玻璃仪器是烧杯、漏斗、玻璃棒,偏铝酸盐能和二氧化碳反应生成氢氧化铝沉淀;
(3)①a中,阴极上氢离子放电生成氢气;
②b中,氢氧化锂和碳酸氢铵反应生成碳酸锂和碳酸铵.
解答:解:(1)根据题意知,酸性条件下,S2O32ˉ被氧化成SO42ˉ,则LiCoO2被氧化生成Co2+,所以发生的离子反应方程式为:S2O32ˉ+8LiCoO2+22H+═2SO42ˉ+8Li++8Co2++11H2O,
故答案为:S2O32ˉ+8LiCoO2+22H+═2SO42ˉ+8Li++8Co2++11H2O;
(2)亚铁离子不稳定,易被氧气氧化生成铁离子,所以除杂时通入空气的目的是将亚铁离子氧化生成铁离子,再将铁离子转化为氢氧化铁沉淀,从而除去亚铁离子;根据表格知,pH为5-6时,铁离子和铝离子完全转化为沉淀,所以废渣的成分是Fe(OH)3、Al(OH)3;分离固体和溶液的方法是过滤,过滤过程中需要的玻璃仪器是烧杯、漏斗、玻璃棒;步骤I中,废渣中的铝和氢氧化钠反应生成偏铝酸钠,步骤II中,向偏铝酸钠溶液中通入过量的二氧化碳,使偏铝酸钠转化为氢氧化铝,反应离子方程式为2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:将Fe2+氧化成Fe3+; Fe(OH)3、Al(OH)3;烧杯、漏斗、玻璃棒;2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ;
(3)①a中,阴极上氢离子放电生成氢气,电极反应式为:2H++2e-═H2↑或2H2O+2e-═H2+2OH-,
故答案为:2H++2e-═H2↑或2H2O+2e-═H2+2OH-;
②b中,氢氧化锂和碳酸氢铵反应生成碳酸锂和碳酸铵,反应方程式为2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3,
故答案为:2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3.
故答案为:S2O32ˉ+8LiCoO2+22H+═2SO42ˉ+8Li++8Co2++11H2O;
(2)亚铁离子不稳定,易被氧气氧化生成铁离子,所以除杂时通入空气的目的是将亚铁离子氧化生成铁离子,再将铁离子转化为氢氧化铁沉淀,从而除去亚铁离子;根据表格知,pH为5-6时,铁离子和铝离子完全转化为沉淀,所以废渣的成分是Fe(OH)3、Al(OH)3;分离固体和溶液的方法是过滤,过滤过程中需要的玻璃仪器是烧杯、漏斗、玻璃棒;步骤I中,废渣中的铝和氢氧化钠反应生成偏铝酸钠,步骤II中,向偏铝酸钠溶液中通入过量的二氧化碳,使偏铝酸钠转化为氢氧化铝,反应离子方程式为2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:将Fe2+氧化成Fe3+; Fe(OH)3、Al(OH)3;烧杯、漏斗、玻璃棒;2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32ˉ或AlO2-+CO2+2H2O═Al(OH)3↓+HCO3ˉ;
(3)①a中,阴极上氢离子放电生成氢气,电极反应式为:2H++2e-═H2↑或2H2O+2e-═H2+2OH-,
故答案为:2H++2e-═H2↑或2H2O+2e-═H2+2OH-;
②b中,氢氧化锂和碳酸氢铵反应生成碳酸锂和碳酸铵,反应方程式为2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3,
故答案为:2LiOH+2NH4HCO3═Li2CO3↓+(NH4)2CO3.
点评:本题考查了离子方程式的书写、电极反应式的书写、氧化还原反应等知识点,难度较大,明确物质的性质是解本题的关键,知道氢氧化铝是重要的两性氢氧化物,能与强酸和强碱反应生成盐.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目



 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 、
、 与
与 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
 在上述溶解过程中,
在上述溶解过程中, 被氧化成
被氧化成 ,
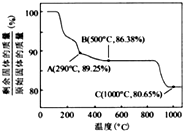
, 在空气中加热时,固体残留率随温度的变化
在空气中加热时,固体残留率随温度的变化