题目内容
(08山东省淄博模拟)(8分)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺,请按要求回答问题:
(1)“氨碱法”产生大量CaC12废弃物,请写出该工艺中产生CaC12的化学方程式:___________。
(2)写出“联合制碱法”有关反应的化验学方程式:____________。
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?________。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%)= 。
答案:(1)2NH4Cl+Ca(OH)2=====2NH3↑+CaCl2+2H2O;
(2)NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl
2NaHCO3=====Na2CO3+ CO2↑+H2O;(1分)
(3)“氨碱法”的CO2来源于石灰石煅烧,“联合制碱法”的CO2来源于合成氨工业的废气。(2分)
(4)由于总反映可看作是:2NH3+2NaCl+CO2+H2O=Na2CO3+2NH4Cl,所以:原子利用率(%)
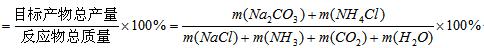

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(08山东省淄博模拟)(18分)在用FeSO4溶液与NaOH溶液反应制备白色的Fe(OH)2时,出现了“白色沉淀迅速转变为灰绿色,最后逐渐变成红褐色”的实验现象,如何解释出现灰绿色的现象,探究小组的同学产生了不同的观点:
①灰绿色物质就是红褐色的氢氧化铁跟白色的氢氧化亚铁的简单混合物;
②灰绿色物质是铁的一种新的氢氧化物,但其中不含Fe3+离子。
(1)验证观点①不正确的实验操作是: ,
验证观点②所需的试剂有: 。
(2)某同学查阅资料后,得到Fe(OH)2如下信息:

阅读该资料后,你对上述实验中出现灰绿色的现象的解释是:__________。
探究小组的同学在研究由Fe2+制备Fe(OH)2的过程中,甲、乙、丙、丁四位同学分别设计了如下4个实验方案:
甲方案:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
乙方案:应用钢铁吸氧腐蚀的原理,设计电池制备Fe(OH)2。
|
丙方案:按图实验,制备Fe(OH)2。 丁方案:按图实验,制备Fe(OH)2。(苯的作用是使电解质溶液隔绝空气)
回答下列问题:
①在甲方案中,所用FeSO4样品通常部分被氧化,写出在配制FeSO4溶液时,其操作过程及反应的离子方程式: 。
②在乙方案中,正极的电极反应式是: 。你认为该方案是否可行? ,若不可行请说明理由(若可行,则该空不需回答): 。
③在丙方案中,当容器B、A中均加入试剂并塞好橡皮塞后,还需要进行的操作是 。
④在丁方案中,在两电极之间的溶液中首先观察到白色沉淀。请写出b电极的电极反应式: 。则其电解质溶液可以是下列三项的 。
A.蒸馏水 B.NaC1溶液 C.NaOH溶液



