题目内容
【题目】碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
(1)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3溶液,两者混合后发生双水解反应生成Al(OH)3和CO2进行灭火,写出该反应的化学方程式_________________________________________________。
(2)Na2O2和NaHCO3都属于钠的化合物,它具有很强的氧化性。少量Na2O2与FeCl2溶液能发生如下反应:____Na2O2+____FeCl2+____H2O→____Fe(OH)3![]() +____FeCl3+____NaCl,已知FeCl2前面系数为6,配平上述化学方程式______,并标出电子转移方向和数目______。该反应中被还原的元素是_________,氧化产物是_________。
+____FeCl3+____NaCl,已知FeCl2前面系数为6,配平上述化学方程式______,并标出电子转移方向和数目______。该反应中被还原的元素是_________,氧化产物是_________。
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中的c(CO32-)的变化是_____(选填“增大”、“减小”或“不变”)。
(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤 ②不通入氨,冷却、加食盐,过滤对两种方法的评价正确的是______(选填编号)。
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
(5)已知HCO3-在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3)___c(CO32-)(选填“>”、“<”、“=”)。
【答案】6NaHCO3+Al2(SO4)3+6H2O→2Al(OH)3↓+6CO2↑+3Na2SO4 3 6 6 4 2 6 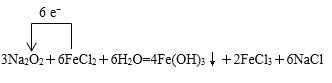
![]() Fe(OH)3和FeCl3 减小 ad >
Fe(OH)3和FeCl3 减小 ad >
【解析】
(1)根据信息,NaHCO3与Al2(SO4)3发生双水解反应,其化学反应方程式为Al2(SO4)3+6NaHCO3+6H2O=2Al(OH)3↓+6CO2↑+3Na2SO4;
(2)Na2O2具有强氧化性,该反应中作氧化剂,Fe2+以还原性为主,作还原剂,Na2O2中O元素共降低2价,Fe2+→Fe3+升高1价,最小公倍数为2,题中给出FeCl2的系数为6,则Na2O2的系数为3,根据原子守恒配平其他,即反应方程式为3Na2O2+6FeCl2+6H2O=4Fe(OH)3↓+2FeCl3+6NaCl;电子转移的方向和数目是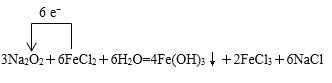 ;该反应中被还原的元素是Na2O2中-1价O,氧化产物是FeCl3和Fe(OH)3;
;该反应中被还原的元素是Na2O2中-1价O,氧化产物是FeCl3和Fe(OH)3;
(3)Ba(OH)2少量,发生离子反应方程式Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32-,NaHCO3电离方程式为NaHCO3=Na++HCO3-,因此加入少许Ba(OH)2固体,溶液中c(CO32-)增大;
(4)a、滤出小苏打后,母液里有NH4Cl和NaHCO3,通入氨气,增加c(NH4+),再加入食盐,使NH4Cl析出,然后过滤,氯化铵的纯度较高,故a说法正确;
b、②中析出的NH4Cl中含有较多的NaCl,氯化铵的纯度降低,故b说法错误;
c、①中滤液还有较多的NH3,不能直接循环使用,故c说法错误;
d、②中滤液中含有较多NaCl,可以直接循环使用,故d说法正确;
(5)HCO3-电离方程式为HCO3-![]() H++CO32-,HCO3-水解方程式HCO3-+H2O
H++CO32-,HCO3-水解方程式HCO3-+H2O![]() H2CO3+OH-,NaHCO3溶液显碱性,说明HCO3-水解程度大于其电离程度,即c(H2CO3)>c(CO32-)。
H2CO3+OH-,NaHCO3溶液显碱性,说明HCO3-水解程度大于其电离程度,即c(H2CO3)>c(CO32-)。