题目内容
已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
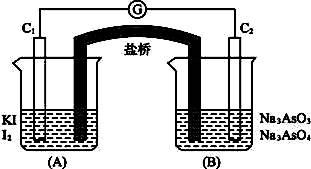
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
(Ⅱ)若改向(B)烧杯中滴加40%NaOH溶液,发现微安表指针偏转方向与Ⅰ相反。
试完成下列问题:
(1)两次操作过程中微安表指针为什么会发生偏转?
(2)两次操作过程中指针偏转方向为什么相反?
 AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
(Ⅱ)若改向(B)烧杯中滴加40%NaOH溶液,发现微安表指针偏转方向与Ⅰ相反。
试完成下列问题:
(1)两次操作过程中微安表指针为什么会发生偏转?
(2)两次操作过程中指针偏转方向为什么相反?
(1)两次操作均发生原电池反应,电流表指针偏转,化学能转变为电能。
(2)由于c(H+)改变,使化学平衡向不同方向移动发生不同方向的反应。
(2)由于c(H+)改变,使化学平衡向不同方向移动发生不同方向的反应。
Ⅰ.操作过程中,C1棒发生的反应为2I--2e-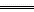 I2
I2
Ⅱ.操作过程中,C2棒发生的反应为AsO33-+H2O-2e-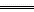 AsO43-+2H+
AsO43-+2H+
总反应为AsO43-+2I-+2H+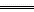 AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。
AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。
Ⅰ操作中(A)池发生氧化反应C1为负极;(B)池中发生还原反应C2为正极。
Ⅱ操作中(A)池发生还原反应C1为正极;(B)池中发生氧化反应C2为负极。
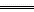 I2
I2Ⅱ.操作过程中,C2棒发生的反应为AsO33-+H2O-2e-
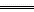 AsO43-+2H+
AsO43-+2H+总反应为AsO43-+2I-+2H+
 AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。
AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。Ⅰ操作中(A)池发生氧化反应C1为负极;(B)池中发生还原反应C2为正极。
Ⅱ操作中(A)池发生还原反应C1为正极;(B)池中发生氧化反应C2为负极。

练习册系列答案
相关题目