题目内容
1.当Mg(OH)2在水中达到溶解平衡时“Mg(OH)2(s)?Mg2+(aq)+20H-(aq),要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是( )| A. | NH4Cl | B. | NaOH | C. | Na2CO3 | D. | Fe |
分析 根据平衡移动原理及溶度积解答,要使Mg (OH)2 固体进一步溶解,即平衡向右移动,可以加水,或降低Mg2+或OH-的浓度.
解答 解:A、加入少量NH4Cl,NH4+与OH-结合生成氨水,故氢氧根的浓度减小,故平衡右移,故A正确;
B、加入NaOH,OH-的浓度增大,平衡向左移动,Mg (OH)2 固体的量增大,故B错误;
C、加入少量Na2C03,CO32-水解生成氢氧根,致使氢氧根浓度增大,平衡左移,Mg (OH)2 固体的量增大,故C错误;
D、加入少量Fe,Fe不溶于水,为金属固体,不改变各种物质的浓度,故D错误;
故选A.
点评 本题主要考查化学平衡的移动,难度不大,注意D选项中铁单质的溶解性以及对溶液中离子浓度的影响.

练习册系列答案
相关题目
11.运用元素周期律分析下面推断,其中错误的是( )
| A. | 硫酸锶(SrSO4)是难溶于水的白色固体 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于酸 | |
| C. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 | |
| D. | 铍(Be)的氧化物的水化物可能具有两性 |
12.碳碳双键不能自由旋转,所以,R-CH=CH-R可能有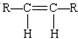 和
和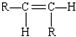 两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
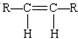 和
和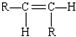 两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )| A. | 丙烯 | B. | 2-戍烯 | C. | 苯乙烯 | D. | 1,3-丁二烯 |
9.下列反应中属于氧化还原反应,但不属于四种基本反应类型的是( )
| A. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+2CO2 | D. | NaOH+HCl═NaCl+H2O |
13.元素X的原子,其M层与K层电子数相同;元素Y的原子,其层上有5个电子.X和Y所形成的稳定化合物的式量为( )
| A. | 100 | B. | 90 | C. | 88 | D. | 80 |
10.乙醇、甘油和苯酚所具有的共同点是( )
| A. | 都易溶于水 | B. | 都能与NaOH溶液反应 | ||
| C. | 分子结构中都含有羟基 | D. | 都属于醇类化合物 |
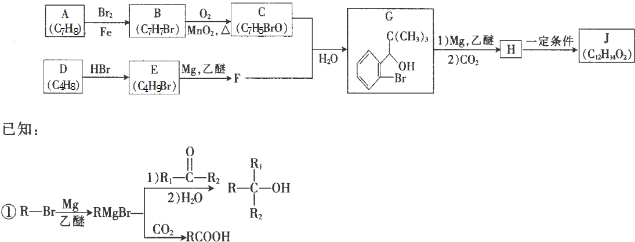
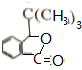 .
.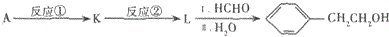
 .
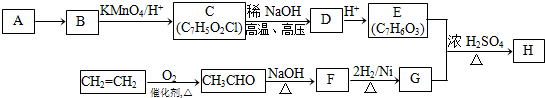
.
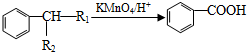 (-R1、-R2表示氢原子或烃基);
(-R1、-R2表示氢原子或烃基);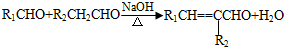 ;
;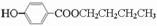 .
.