题目内容
7.对于反应A+B-→C,如果温度每升高10℃,反应速率增加为原来的3倍.在10℃时,完成反应的20%需要54min;将温度提高到40℃,完成反应的20%需要的时间为( )| A. | 2 min | B. | 3 min | C. | 6 min | D. | 9 min |
分析 已知温度每升高10℃,化学反应速率增大到原来的3倍,那么10℃时,温度升高40℃,反应速率应是10℃的33=27倍,以此解答该题.
解答 解:已知温度每升高10℃,化学反应速率增大到原来的3倍,那么10℃时,温度提高到40℃,反应速率应是10℃的33=27倍,在10℃时,完成反应的20%需要54min,则温度提高到40℃完成反应的20%需要时间(min)为$\frac{54min}{27}$=2min,故选A.
点评 本题考查反应速率的影响因素,侧重于分析与应用能力的考查,题目难度不大,注意温度升高后速率的变化倍数为解答该类题目的关键.

练习册系列答案
相关题目
17.下列化学反应的离子方程式正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 用CH3 COOH溶解CaC03:CaCO3+2H+═Ca++H2O+CO2↑ | |
| C. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4↓+AlO${\;}_{2}^{-}$+2H2O | |
| D. | 用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O |
18. 阅读、分析下列两个材料:
阅读、分析下列两个材料:
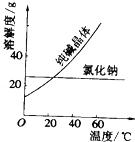
材料一(如图):
材料二:
选择回答下列问题(填写序号):A.分液法 B.“溶解成热饱和溶液、冷却结晶、过滤”的方法 C.“溶解、蒸发结晶、趁热过滤”的方法 D.蒸馏法 E.过滤法 F.萃取法
①将乙二醇和丙三醇相互分离的最佳方法是D.
②提取碘水中的碘,可综合选用上述三种方法依次是F、A、D.
③将含有氯化钠杂质的纯碱提纯出来,最好应用B.
 阅读、分析下列两个材料:
阅读、分析下列两个材料:材料一(如图):
材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
①将乙二醇和丙三醇相互分离的最佳方法是D.
②提取碘水中的碘,可综合选用上述三种方法依次是F、A、D.
③将含有氯化钠杂质的纯碱提纯出来,最好应用B.
15.在酸性溶液中,下列各组离子能大量共存的是( )
| A. | NH${\;}_{4}^{+}$、K+、Al3+、SO${\;}_{4}^{2-}$ | B. | Cl-、I-、K+、MnO${\;}_{4}^{-}$ | ||
| C. | Na+、S2O${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$、K+ | D. | Na+、NO${\;}_{3}^{-}$、PO${\;}_{4}^{3-}$、Cl- |
2.催化剂的研究是化学反应原理中的一个重要领域,下列有关叙述正确的是( )
| A. | 加催化剂可以增大或减小化学反应的焓变 | |
| B. | 催化剂能降低反应所需活化能 | |
| C. | 任何化学反应都需要活化能的推动 | |
| D. | 对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比例 |
12.MgBr2和MgO的混合物共10g,经分析,其中Mg元素的质量分数为38.4%,则Br元素的质量分数为( )
| A. | 30% | B. | 40% | C. | 50% | D. | 46% |
19.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA | |
| B. | 64g SO2含有NA个SO2分子 | |
| C. | 16g CH4所含的电子数为NA | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
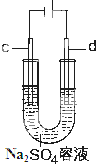 在25℃时,将一根石墨棒和一根铁棒做两电极分别插入一定量的硫酸钠饱和溶液中进行电解(见图),
在25℃时,将一根石墨棒和一根铁棒做两电极分别插入一定量的硫酸钠饱和溶液中进行电解(见图),