题目内容
某有机物的组成为碳52.25%、氢13%,该有机物1 g与足量金属钠反应,标状况下放出0.243 L H2,则该有机物的结构简式为
- A.C2H5OH
- B.CH3CH2CH2OH
- C.CH3OH
- D.C4H9OH
A
根据产生H2的体积计算出醇的物质的量n=2×0.243 L/22.4 L/mol=0.022 molM="1" g/0.022 mol=45.5 g/mol分子中含碳原子数=45.5×52.25%/12=2分子中含氢原子数=45.5×13%/1=6分子中含氧原子数=45.5—12×2—1/16=1所以分子式为C2H6O,故选A。
根据产生H2的体积计算出醇的物质的量n=2×0.243 L/22.4 L/mol=0.022 molM="1" g/0.022 mol=45.5 g/mol分子中含碳原子数=45.5×52.25%/12=2分子中含氢原子数=45.5×13%/1=6分子中含氧原子数=45.5—12×2—1/16=1所以分子式为C2H6O,故选A。

练习册系列答案
相关题目
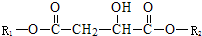 (其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
(其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化: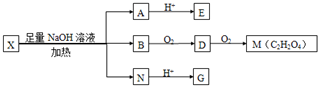



 、
、 、
、
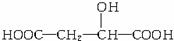
 (其中I、II为未知部分的结构)
(其中I、II为未知部分的结构)