题目内容
0.05 mol某金属单质与足量的盐酸反应,放出1.12L H2(标准状况),并转变为具有Ar原子的电子层结构的离子,该金属元素在元素周期表中的位置是:( )
| A.第三周期第IA族 | B.第四周期第IA族 | C.第三周期第ⅡA族 | D.第四周期第ⅡA族 |
D
1.12L H2是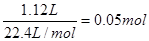 ,所以转移电子的物质的量为0.05mol×2=0.1mol。根据得失电子守恒可知金属的化合价为
,所以转移电子的物质的量为0.05mol×2=0.1mol。根据得失电子守恒可知金属的化合价为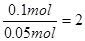 ,又因为金属离子具有Ar原子的电子层结构,所以该金属的原子序数为18+2=20,即为钙元素。所以答案是D。
,又因为金属离子具有Ar原子的电子层结构,所以该金属的原子序数为18+2=20,即为钙元素。所以答案是D。
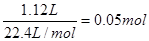 ,所以转移电子的物质的量为0.05mol×2=0.1mol。根据得失电子守恒可知金属的化合价为
,所以转移电子的物质的量为0.05mol×2=0.1mol。根据得失电子守恒可知金属的化合价为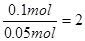 ,又因为金属离子具有Ar原子的电子层结构,所以该金属的原子序数为18+2=20,即为钙元素。所以答案是D。
,又因为金属离子具有Ar原子的电子层结构,所以该金属的原子序数为18+2=20,即为钙元素。所以答案是D。
练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目