题目内容
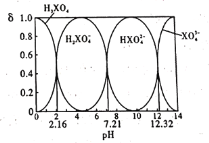
【题目】某酸在水溶液中,四种微粒的物质的量分数(δ)随溶液pH的变化曲线如图所示。下列说法正确的是
A.H3XO4为三元弱酸,NaH2XO4溶液呈碱性
B.-lgKa3=12.32
C.向0.1 mol/L的Na3XO4溶液中滴加几滴浓KOH溶液,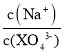 的值变大
的值变大
D.0.1 mol/L的Na2HXO4溶液中,c(Na+)+c(H+)=c(XO43-)+c(HXO42-)+c(H2XO4-)+c(OH-)
【答案】B
【解析】
A.H3XO4能最终电离生成XO43-,说明H3XO4为三元弱酸;当pH=2.16时,溶液中c(H3XO4)=c(H2XO4-),则Ka1=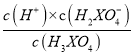 =10-2.16,此时Kh3=
=10-2.16,此时Kh3=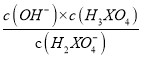 =
=![]() =
=![]() =10-11.84<Ka1;当pH=7.21时,溶液中c(HXO42-)=c(H2XO4-),则Ka2=
=10-11.84<Ka1;当pH=7.21时,溶液中c(HXO42-)=c(H2XO4-),则Ka2=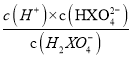 =10-7.21>Kh3,即NaH2XO4溶液中,H2XO4-的电离程度大于H2XO4-的水解程度,溶液呈酸性,故A错误;
=10-7.21>Kh3,即NaH2XO4溶液中,H2XO4-的电离程度大于H2XO4-的水解程度,溶液呈酸性,故A错误;
B.当pH=12.32时,溶液中c(XO43-)=c(HXO4-),则Ka3=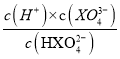 =10-12.32,则-lgKa3=12.32,故B正确;
=10-12.32,则-lgKa3=12.32,故B正确;
C.向0.1 mol/L的Na3XO4溶液中滴加几滴浓KOH溶液,抑制XO43-的水解,溶液中XO43-的数目增大,而Na+数目不变,则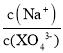 =
=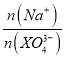 的比值减小,故C错误;
的比值减小,故C错误;
D.在0.1 mol/L的Na2HXO4溶液中存在的电离守恒式为c(Na+)+c(H+)=3c(XO43-)+2c(HXO42-)+c(H2XO4-)+c(OH-),故D错误;
故答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目