题目内容
【题目】(9分)认真观察下列装置,回答下列问题:
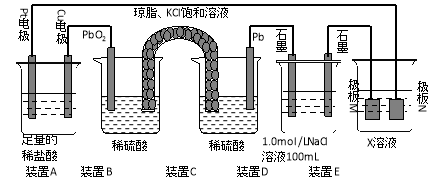
⑴装置B中PbO2上发生的电极反应方程式为 。
⑵装置A中总反应的离子方程式为 。
⑶若装置E中的目的是在Cu材料上镀银,则X为 ,极板N的材料为 。
若装置E的目的是验证金属的电化学防腐,则极板N的材料为__________________ 。
⑷当装置A中Cu电极质量改变6.4g时,装置D中产生的气体体积为 L(标准状况下)。
【答案】⑴PbO2+4H++SO2- 4+2e-=PbSO4+2H2O (2分)
⑵Cu+2H+![]() Cu2++H2↑(2分)
Cu2++H2↑(2分)
⑶AgNO3 Ag 惰性电极(或石墨等不溶性惰性材料)(各1分) ⑷3.92(2分)
【解析】(1)根据装置图可判断,BC是原电池,二氧化铅是正极,得到电子,电极反应式为PbO2+4H++SO2- 4+2e-=PbSO4+2H2O。
(2)A中铜电极和正极相连,是阳极,铜失去电子。阴极是Pt,溶液中的氢离子得到电子,所以总的反应式为Cu+2H+![]() Cu2++H2↑。
Cu2++H2↑。
(3)电镀时镀层金属作阳极,待镀金属作阴极,含有镀层金属离子的溶液作电镀液,所以X是硝酸银溶液。N是阳极,则N是银。由于N是阳极,所以如果装置E的目的是验证金属的电化学防腐,则极板N的材料应为惰性电极。
(4)当装置A中Cu电极质量改变6.4g时,转移电子是6.4g÷64g/mol×2=0.2mol。装置D中氯化钠是0.1mol,阴极是氢离子放电,氢气是0.1mol。阳极是氯离子放电,生成氯气,物质的量是0.05mol,所以阴极还生成氧气,物质的量是0.1mol÷4=0.025mol,
所以标准状况下的体积共计是(0.1mol+0.05mol+0.025mol)×22.4L/mol=3.92L.。

练习册系列答案
相关题目