题目内容
硝酸是一种重要的工业原料,工业制硝酸的关键是氨的催化氧化,与硝酸工业相关的过
程中产生的氮氧化物的处理与应用也是科学研究的热点。
I.甲、乙分别是实验室模拟合成氨及氨催化氧化的装置
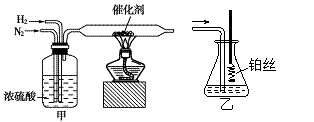 |
⑴ 氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有控制气体流速、 ▲ 。
⑵ 用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,铂丝保
持红热的原因是 ▲ ,写出乙装置中氨氧化的化学方程式 ▲ 。反应结束后锥形瓶内的溶
液中含有H+、OH-、 ▲ 、 ▲ 离子。
II.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
⑴ 工业上常用Na2CO3溶液吸收法处理NOx 。
已知:NO不能与Na2CO3溶液反应
NO + NO2 + Na2CO3 = 2NaNO2 + CO2 ①
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2 ②
当NOx被Na2CO3溶液完全吸收时,x的值不可能是 ▲ (填字母)。
A.1.3 B.1.6 C.1.8
⑵ 尿素也可用于吸收处理NOx,其反应原理为:
NO+NO2+H2O=2HNO2
2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
当混合气体中NO、NO2按上述反应中系数比时吸收效果最佳。若混合气体中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)= ▲ (空气中氧气的体积含量约为20%)。
I.(1)干燥混合气体 (1分)
(2)氨的氧化反应是一个放热反应 (2分); 4NH3十5O2![]() 4NO+6H2O。(2分)
4NO+6H2O。(2分)
NH4+ (1分), NO3- (1分)
II.(1)A (2分) (2)1:1(2分)

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A、硝酸见光易分解,应保存在棕色试剂瓶中 | B、常温下,Al、Fe等金属不能在稀硝酸中溶解 | C、硝酸能和某些有机物发生硝化、磺化、酯化反应 | D、将浓硝酸和浓盐酸按体积比3:1混合得到比硝酸氧化性更强的王水 |