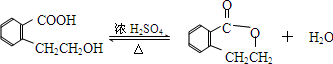题目内容
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p亚层中有3个电子。
(1)C原子的基态电子排布式为_______________,若A元素的原子最外层电子排布为1s1,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于____ _键。
(2)当n=2时,元素A在周期表中的位置是______________________,属于_____区元素;
B的原子结构示意图为________ __,B与C形成的化合物的电子式为______________。
(3)当n=3时,B与C形成的晶体中微粒间的作用力是________ __,此时 A、B、C、D四种元素的第一电离能由大到小的顺序是__________________(用元素符号表示)。
⑴ 1s22s22p4 σ
⑵ 第二周期第ⅠA族 s C原子结构示意图 CO2的电子式
⑶共价键(或极性共价键) O> P > Si > Na
解析:略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
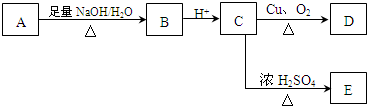
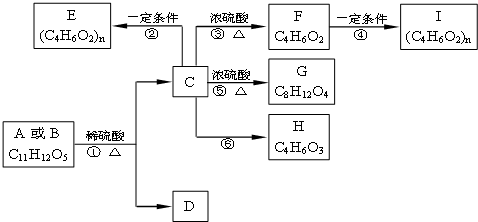
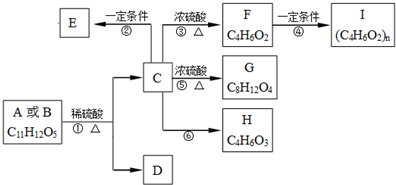
 ,现有A、B、C、D、E、F、G、H八种有机物,存在如下图所示的转化关系:
,现有A、B、C、D、E、F、G、H八种有机物,存在如下图所示的转化关系:


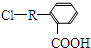 (其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.
(其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.