题目内容
把6.9 g钠和4.2 g硅同时投入足量水中,充分反应后,测得溶液体积为500 mL,计算标准状况下产生氢气的体积是多少升?所得溶液中溶质的物质的量浓度是多少?(提示:Si+2NaOH+H2O![]() Na2SiO3+2H2↑)
Na2SiO3+2H2↑)
解析:
|
答案:10.08 L 0.3 mol·L-1 解析:先根据 2Na+2H2O 2 mol 2 mol 1 mol 6.9 g/23(g·L-1)=0.3 mol 0.3 mol 0.15 mol 再根据Si+2NaOH+H2O 1 mol 2 mol 1 mol 2 mol 4.2 g/28 g·L-1) 0.3 mol 0.15 mol 0.3 mol 则V(H2)=(0.15 mol+0.3 mol)×22.4 L·mol-1=10.08 L c(Na2SO3)=0.15 mol/0.5 L=0.3 mol·L-1 |

实验序号 | 实验方案 | 实验现象 |
1 | 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 | 反应激烈,有大量气体产生,并能使木条复燃 |
2 | 将实验1所得溶液分成两份,一份加入紫色石蕊试液;一份加入无色酚酞试液 | 溶液变蓝,且长时间不褪色 溶液显红色,半分钟内褪色 |
3 | 若把实验1所得溶液分成两份。一份加热至沸1~2 min,再滴入酚酞试液;另一份加热至沸1~2min,再滴入紫色石蕊试液 | 溶液显红色,但仍很慢褪色 溶液显蓝色,且很快褪色 |
4 | 在变为蓝色石蕊试液中滴加H2O2溶液加热至沸 | 蓝色褪去 |
5 | 若把实验1所得溶液中加入少许MnO2,静置到无气体产生时,分成两份 一份加入无色酚酞加热至沸? 一份加入紫色石蕊加热至沸 | 溶液变红,且不再褪色 溶液变蓝,且不再褪色 |
6 | ①称取 ②待不再产生气体,10 min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触 | 测得氧气体积为170 mL左右(已转换成标准状况下体积且已考虑50 mL水和导气管中水两者所占容积的体积因素)? 又产生大量氧气,至反应完全以后,又测得产生了390 mL氧气(已转换成标准状况下体积且两次测定条件均相同) |
请仔细阅读有关内容后完成问题:?
(1)根据实验分析,过氧化钠与水反应除了课本所介绍的上述反应外还存在另一反应,其化学方程式为________________。?
(2)写出实验5中“加入少许MnO2产生气体”时所发生反应的化学方程式:________________________。?
(3)从以上实验结果分析,石蕊分子与酚酞分子相比较,它们的稳定性________(填“相等”“前者大”或“后者大”)。?
(4)综合分析上述实验,指出使变红的酚酞褪色的物质是________,从此实验你认为该物质具有哪些性质________________________________________。?
(5)若气体流向从左到右,将完成实验6所需仪器填入表中并连接好。
A | B | C |
|
|
|
某中学学生将过氧化钠与水的反应作为研究性学习的课题。他们经过查资料、提出假设、进行实验设计,并通过实验得到结论验证。下表是他们的实验方案及实验现象。
| 实验 序号 | 实验方案 | 实验现象 | ||||
| 1 | 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 | 反应激烈,有大量气体产生,并能使木条复燃 | ||||
| 2 | 将实验1所得溶液分成两份: 一份加入紫色石蕊试液 另一份加入无色酚酞试液 | 溶液变蓝且长时间不褪色 溶液显红色,半分钟内褪色 | ||||
| 3 | 若把实验1所得溶液分成两份: 一份加热至沸1min~2min,再滴入酚酞试液 另一份加热至沸1 min~2min,再滴入紫色石蕊试液 | 溶液显红色,但仍很快褪色 溶液显蓝色且很快褪色 | ||||
| 4 | 在变为蓝色石蕊试液中滴加H2O2溶液加热至沸 | 蓝色褪去 | ||||
| 5 | 若把实验1所得溶液中加入少许MnO2,静置到无气体产生时,分成两份。 一份加入无色酚酞加热至沸 一份加入紫色石蕊加热至沸 | 溶液变红且不再褪色 溶液变蓝且不再褪色 | ||||
| 6 | ①称取3.9 g过氧化钠固体,逐滴加入约50mL水 ②待不再产生气体,10 min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触 | 测得氧气体积为170mL左右(已转换成标准状况下体积且已考虑50 mL水和导气管中水两者所占容积的体积因素) 又产生大量氧气,至反应完全以后,又测得产生了390 mL氧气(已转换成标准状况下体积且两次测定条件均相同) | ||||
请仔细阅读有关内容后回答:
(1)根据实验分析,过氧化钠与水反应除了课本所介绍的上述反应外还存在另一反应,其化学方程式为:
(2)写出实验5中“加入少许MnO2产生气体”时所发生反应的化学方程式:
(3)从以上实验结果分析,石蕊分子与酚酞分子相比较,它们的稳定性 (填“相等”、“前者大”或“后者大”)。
(4)综合分析上述实验,指出使变红的酚酞褪色的物质是 ,从此实验你认为该物质具有哪些性质
(5)若气体流向从左到右,将完成实验6所需仪器填入表中并连接好。

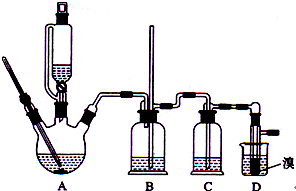 (2012?海南)实验室制备1,2-二溴乙烷的反应原理如下:
(2012?海南)实验室制备1,2-二溴乙烷的反应原理如下: