题目内容
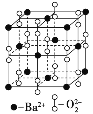
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列有关说法中正确的是
A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体的晶胞结构与CsCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
【答案】AD
【解析】
A.Ba元素是活泼金属元素,O元素是活泼非金属元素,该晶体中的微粒为Ba2+和O22-,钡在氧气中燃烧时得到一种钡的氧化物属于离子晶体,A正确;
B.晶胞中Ba2+离子位于晶胞的顶点和面心位置,晶胞中共含有Ba2+离子的个数为8×![]() +6×
+6×![]() =4,阴离子位于晶胞的边上和体心位置,共含有阴离子的个数为12×
=4,阴离子位于晶胞的边上和体心位置,共含有阴离子的个数为12×![]() +1=4,所以晶胞中Ba2+与阴离子的个数比为1:1,该氧化物为BaO2,B错误;
+1=4,所以晶胞中Ba2+与阴离子的个数比为1:1,该氧化物为BaO2,B错误;
C.由晶胞结构可知,离子配位数为6,与NaCl结构相似,而CsCl晶体中离子的配位数是8, C错误;
D.以顶点Ba2+离子为研究对象,与之距离相等且最近的Ba2+位于面心上,位于顶点的Ba2+被8个晶胞共用,位于面心上的Ba2+被2个晶胞共用,故与每个Ba2+距离相等且最近的Ba2+共有![]() =12个,D正确;
=12个,D正确;
故合理选项是AD。

练习册系列答案
相关题目