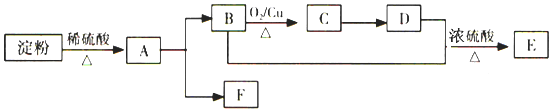
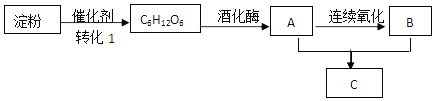
题目内容
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱。则可将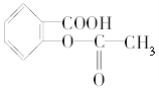 转变为
转变为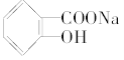 的方法是( )
的方法是( )
①与足量的NaOH溶液共热,再通入CO2 ②与稀硫酸共热后,加入足量的NaOH溶液 ③加热溶液,通入足量的SO2 ④与稀H2SO4共热后,加入足量的NaHCO3
A.①②
B.①④
C.②③
D.②④
【答案】B
【解析】
①.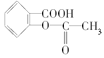 与足量的NaOH溶液共热,生成
与足量的NaOH溶液共热,生成![]() ,根据酸性强弱顺序,在
,根据酸性强弱顺序,在![]() 溶液中通入足量CO2,可得到
溶液中通入足量CO2,可得到![]() ,①符合题意;
,①符合题意;
②.  与稀硫酸共热后,生成
与稀硫酸共热后,生成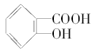 ,加入足量的NaOH溶液,反应生成
,加入足量的NaOH溶液,反应生成![]() ,②不合题意;
,②不合题意;
③.加热溶液,通入足量的SO2,SO2与水反应生成H2SO3,其酸性比醋酸强,所以发生反应,生成 ,③不合题意;
,③不合题意;
④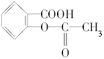 与稀H2SO4共热后生成
与稀H2SO4共热后生成 ,苯酚不能与NaHCO3反应,苯甲酸能与NaHCO3反应,则
,苯酚不能与NaHCO3反应,苯甲酸能与NaHCO3反应,则 与NaHCO3反应,生成
与NaHCO3反应,生成 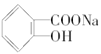 ,④符合题意。
,④符合题意。
综合以上分析,①④符合题意。故选B。

【题目】实现碳及其化合物的相互转化,对开发新能源和降低碳排放意义重大。
(1)已知:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=x
CO(g)+3H2(g) △H=x
已知:标准状态下,由最稳定的单质生成1mol化合物的焓变,称为该化合物的标准摩尔生成焓,几种物质的标准摩尔生成焓如下。则x=__kJ·mol-1。(标准摩尔生成焓:CH4(g)-75kJ/mol;H2O(g)-240kJ/mol;CO(g)-110kJ/mol;H2(g)-0kJ/mol)
(2)为了探究温度、压强对反应(1)的影响,在恒温恒容下,向下列三个容器中均充入4molCH4和4molH2O。
容器 | 温度/℃ | 体积/L | CH4平衡浓度/mol·L-1 | 平衡时间/min |
甲 | 400 | 1 | 1.5 | 5.0 |
乙 | 500 | 1 | x | t1 |
丙 | 400 | 2 | y | t2 |
①平衡前,容器甲中反应的平均速率![]() (H2)=__mol/(L·min);在一定条件下,能判断容器丙中的反应一定处于化学平衡状态的是__(填序号);
(H2)=__mol/(L·min);在一定条件下,能判断容器丙中的反应一定处于化学平衡状态的是__(填序号);
A.3v(CH4)正=v(H2)逆 B.CH4和H2O的转化率相等
C.容器内压强保持不变 D.混合气体的密度保持不变
②平衡后,乙容器中CH4的转换率较丙低,其原因是__,其中t1__t2(填“>”、 “<”或“=”)。
(3)pC是指极稀溶液中溶质物质的量浓度的负对数。已知常温下,H2CO3溶液中加入强酸或强碱后达到平衡时溶液中三种成分的pC-pH图,据图
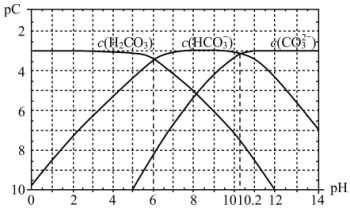
常温下,碳酸的一级电离常数Ka1的数量级为__;其中碳酸的Ka1>>Ka2,其原因是__。
(4)我国科学家根据反应CO2![]() C+O2↑,结合电解池原理设计出了二氧化碳捕获与转化装置。该装置首先利用电解池中熔融电解质ZrO捕获CO2,发生的相关反应为:①CO2+O2-=CO32-,②2CO2+O2-=C2O52-,然后CO32-在阴极转化为碳单质和__;C2O52-在阳极发生电极反应,其方程式为__。
C+O2↑,结合电解池原理设计出了二氧化碳捕获与转化装置。该装置首先利用电解池中熔融电解质ZrO捕获CO2,发生的相关反应为:①CO2+O2-=CO32-,②2CO2+O2-=C2O52-,然后CO32-在阴极转化为碳单质和__;C2O52-在阳极发生电极反应,其方程式为__。