题目内容
下列解释事实的方程式不准确的是
| A.绿矾久存,表面变黄褐色:4(FeSO4·7H2O)+O2=4Fe(OH)SO4+26H2O |
| B.不能用玻璃塞试剂瓶盛放强碱性溶液:SiO2+2OH-=SiO32-+H2O |
| C.淡黄色的过氧化钠粉末久存,表面变白:2Na2O2=2Na2O+O2 |
| D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
C
解析试题分析:过氧化钠粉末久存,表面变白原因是:先与水反应生成氢氧化钠,氢氧化钠吸水潮解形成溶液,再吸收空气中的二氧化碳,得到碳酸钠溶液,溶液失水形成碳酸钠晶体,晶体风化,最后得到碳酸钠粉末。
考点:考查物质的保存、变质等知识。

练习册系列答案
相关题目
下列各组描述正确的是
| A.化工生产要遵守三原则:充分利用原料、充分利用能量、保护环境。①燃烧时使用沸腾炉②制盐酸时将氯气在氢气中燃烧③制硫酸时使用热交换器这3种化工生产分别符合以上某原则 |
| B.① 用燃烧的方法鉴别甲烷、乙烯和乙炔②用酒精萃取溴水中的溴③ 用水鉴别硝酸铵和氢氧化钠固体④用互滴法鉴别Na2CO3、盐酸、BaCl2、NaCl四种溶液以上均能达到实验目的 |
| C.①用硫粉覆盖地下撒有的汞②金属钠着火用泡沫灭火器或干粉灭火器扑灭③用热碱溶液洗去试管内壁的硫④用湿的红色石蕊试纸检验氨气是否集满以上操作均合理 |
| D.①过氧化氢:火箭燃料②碳酸氢钠:食品发酵剂③钠:制氢氧化钠④硫酸:制蓄电池以上物质的用途均合理 |
下列现象或事实可以用同一原理解释的是( )
| A.将少量品红溶液分别滴入浓硝酸中和氯水中 |
| B.漂白粉及水玻璃长期暴露于空气中而变质 |
| C.酸性高锰酸钾溶液与亚硫酸钠溶液混合后褪色及硫酸铁溶液与淀粉碘化钾溶液混合后变蓝 |
| D.将适量Na2O2和Na分别加入硫酸亚铁溶液中;都能得到红褐色沉淀 |
五颜六色的变化增添了化学的魅力。下列有关反应的颜色变化叙述:
①新制氯水久置后→无色;②淀粉溶液遇单质碘→蓝色;③溴化银见光分解→银白色;④热的氧化铜遇乙醇→红色;⑤硝酸银溶液和碘化钾溶液产生沉淀→黄色;⑥苯酚在空气中被氧化→粉红色。其中正确的是
| A.①②④⑤⑥ | B.②③④⑤⑥ | C.①②③④⑤ | D.①④⑤⑥ |
下列说法错误的是( )
| A.SO2通入BaCl2溶液中无沉淀产生,通入FeCl3和BaCl2的混合溶液中有白色沉淀生成 |
| B.红磷在氯气中燃烧产生白色烟雾 |
| C.氯化碘(ICl)的化学性质与氯气相似,它跟水反应可生成HI和HClO |
| D.可在NaOH溶液液面上用倒扣漏斗装置吸收残余氯气 |
下列图中的实验方案,能达到实验目的的是
| | A | B | C | D |
| 实验方案 | 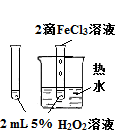 |  将NO2球浸泡在冰水和热水中 |  | 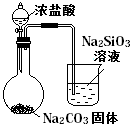 |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 探究温度对平衡 2NO2  N2O4的影响 N2O4的影响 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①过量Na2O2投入到FeCl2溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2SiO3溶液中通入过量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
| A.全部 | B.①⑤ | C.②③④ | D.②③④⑤ |
下列叙述不正确的( )
| A.金属材料分为黑色金属材料和有色金属材料 |
| B.活泼金属在空气中易与氧气反应,表面生成一层氧化膜均能保护内层金属 |
| C.硅是一种亲氧元素,在自然界中它总是与氧相互化合的 |
| D.氯是最重要的“成盐元素”,主要以NaCl的形成存在于海水和陆地的盐矿中 |
下列各组物质能按“→”所示关系实现转化的是(“→”表示反应一步完成)
| A.Al→Al2O3→NaAlO2→Al(OH)3 |
| B.Si→SiO2→H2SiO3→Na2SiO3 |
| C.N2→NO2→HNO3→NO |
D. |