题目内容
【题目】KClO3和浓盐酸在一定温度下反应可表示为
____KClO3+____HCl(浓)=____KCl+____ClO2↑+____Cl2↑+____H2O
(1)请配平上述化学方程式。
(2)标出电子转移方向和数目
(3)氧化剂是,还原产物是。(写化学式)
(4)浓盐酸在反应中显示出来的性质是________(填编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(5)产生0.1molCl2,转移电子的物质的量为________mol。
【答案】
(1)2,4,2,2,1,2;
(2) ;
;
(3)KClO3;ClO2
(4)②;
(5)0.2
【解析】(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;所以KClO3系数为2,KCl系数为2,HCl系数为4,水的系数是2,故答案为:2;4;2;2;1;2;
(2)电子转移的方向和数目为:![]() ,故答案为:
,故答案为: ;
;
(3)KClO3中氯元素化合价由+5价降低为ClO2中+4价,KClO3为氧化剂,还原产物是ClO2,故答案为:KClO3;ClO2;
(4)反应2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O中,HCl中氯元素化合价由-1价升高为Cl2中0价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半,故选:②;
(5)反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,所以产生0.1molCl2,转移的电子的物质的量为0.1mol×2=0.2mol,故答案为:0.2。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案【题目】反应:MgSO4(s) + CO(g)![]() MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
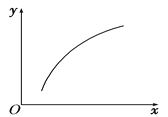
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
