题目内容
【题目】氮元素的单质和常见的化合物在工、农业生产中用途广泛.
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是____________;
(2)雷雨时空气中的N2转化为NO,生成物NO是______色的气体,________(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应. NO2与水反应的化学方程式为_______________________________;
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为_____________________________;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为______g;
(4)已知:4NH3+6NO![]() 5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.
5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.
![]()
将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液.NH3与稀硫酸溶液反应的化学方程式为____________________________________________;
【答案】N2(氮气) 无 难 3NO2+H2O=2HNO3+NO 2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑ 10.7 2NH3+H2SO4===(NH4)2SO4
CaCl2+2H2O+2NH3↑ 10.7 2NH3+H2SO4===(NH4)2SO4
【解析】
(1)逐渐升温的过程中,沸点低的物质先分离,由表可知,最先分离出来的气体时N2;
(2)NO为无色气体;难溶于水;NO2与H2O反应生成硝酸和NO,且反应方程式为:3NO2+H2O=2HNO3+NO;
(3)固体NH4Cl与固体Ca(OH)2加热反应制取氨气,其反应方程式为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑;若要制取标准状况下4.48L的氨气,即0.2molNH3,至少需要0.2molNH4Cl,其质量
CaCl2+2H2O+2NH3↑;若要制取标准状况下4.48L的氨气,即0.2molNH3,至少需要0.2molNH4Cl,其质量![]() ;
;
(4)NH3属于碱性气体,与稀硫酸反应的化学方程式为:2NH3+H2SO4===(NH4)2SO4。

 步步高达标卷系列答案
步步高达标卷系列答案【题目】以高氯冶炼烟灰(主要成分为铜锌的氯化物、氧化物、硫酸盐,少量铁元素和砷元素)为原料,可回收制备Cu和ZnSO4H2O,其主要实验流程如下:
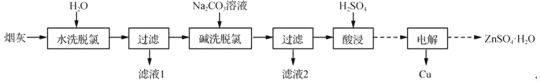
已知:①Fe3+完全沉淀pH为3.2,此时Zn2+、Cu2+未开始沉淀;
②K3[Fe(CN)6]可用于检验Fe2+:3Fe2++2[Fe(CN)6]3﹣═Fe3[Fe(CN)6]2↓(深蓝色);
③砷元素进入水体中对环境污染大,可通过沉淀法除去。
(1)两段脱氯均需在85℃条件下进行,适宜的加热方式为_____。
(2)碱洗脱氯时,溶液中Cu2+主要转化为Cu(OH)2和Cu2(OH)2CO3,也会发生副反应得到Cu2(OH)3Cl沉淀并放出气体,该副反应的离子方程式为_____。若用NaOH溶液进行碱洗操作时,浓度不宜过大,通过下表的数据分析其原因是_____。
NaOH溶液浓度对脱氯率和其他元素浸出率的影响
NaOH浓度/molL﹣1 | 脱氯率/% | 元素浸出率/% | ||
Cl | Zn | Cu | As | |
1.0 | 51.20 | 0.51 | 0.04 | 0.00 |
2.0 | 80.25 | 0.89 | 0.06 | 58.87 |
3.0 | 86.58 | 7.39 | 0.26 | 78.22 |
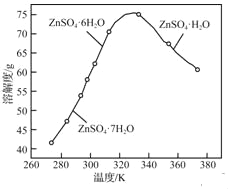
(3)ZnSO4的溶解度曲线如下图所示。“电解”后,从溶液中回收ZnSO4H2O的实验、操作为_____。
(4)滤液1和滤液2中含一定量的Cu2+、Zn2+.为提高原料利用率,可采取的措施有:将滤液1和滤液2混合,回收铜锌沉淀物;循环使用电解过程产生的_____(填化学式)。
(5)已知H3AsO3的还原性强于Fe2+,Ksp(FeAsO3)>Ksp(FeAsO4)=5.7×10﹣21.测得酸浸液中杂质铁元素(以Fe2+存在











