题目内容
【题目】氮化铝(AlN)是一种新型无机非金属材料.为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中A1N的含量,某实验小组设计了如下两种实验方案.
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案l】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).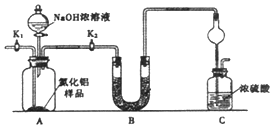
(1)如图C装置中球形干燥管的作用是 .
(2)完成以下实验步骤:组装好实验装置后,首先 ,
再加入实验药品.接下来关闭K1 , 打开K2 , 打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是 .
(3)装置B中试剂可以为(选正确序号填空).
①浓硫酸 ②碱石灰 ③P2O5④还原铁粉
若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”).由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 .
(4)【方案2】按以下步骤测定样品中A1N的纯度: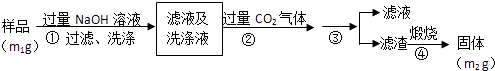
步骤②生成沉淀的离子方程式为 .
步骤③的操作是 . A1N的纯度是 (用m1、m2表示).
【答案】
(1)防止倒吸
(2)检查装置气密性;把装置中残留的氨气全部赶入C装置
(3)②;偏高;C装置出口处连接一个干燥装置
(4)CO2+AlO2﹣+2H2O=HCO3﹣+Al(OH)3↓;过滤、洗涤;![]() ×100%
×100%
【解析】解:【方案1】(1)氨气是与浓硫酸能发生反应的气体,易发生倒吸,图C装置中球形干燥管的作用是防止倒吸的作用,
所以答案是:防止倒吸;(2)组装好实验装置,气体制备需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1 , 打开K2 , 打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是,反应生成氨气后把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算,
所以答案是:检查装置气密性;把装置中残留的氨气全部赶入C装置;(3)装置B是干燥氨气,选择碱石灰,选②,若去掉装置B,测定氨气含量会增大,导致AlN的含量测定结果偏高,装置存在缺陷是空气中的水蒸气也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管;
所以答案是:②;偏高;C装置出口处连接一个干燥装置;