题目内容
【题目】利用电化学原理可以解决很多问题。
(1)精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中常用的银电量计结构如图所示。
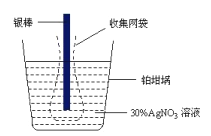
①电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是_____________;
②实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会____________(填“偏高"“偏低”或“无影响”);
③若要测定电解精炼铜时通过的电量,可将该银电量计中的银棒与待测电解池的________电极相连。
(2)如图所示,将铁棒和石墨棒插人盛有饱和NaCl溶液的U型管中。

①K1闭合,铁棒上发生的反应为______________;
②K2闭合,铁棒不会被腐蚀,属于_________保护法。
【答案】
(1)①Ag++e-=Ag②偏高;③精铜
(2)①Fe-2e=Fe2+;②外加电流的阴极保护法
【解析】
试题分析:(1)①应该使Ag作阳极,连接电源的正极相连,发生反应:Ag-e-=Ag+,铂坩埚与电源的负极相连,作阴极,铂坩埚上发生的电极反应是:Ag++e-=Ag,故答案为:Ag++e-=Ag;
②银溶解时有些可能未失电子变成银离子,然后在阴极(铂坩埚)得电子析出,而是直接跌落到铂坩埚中,造成铂坩埚增重较多,导致计算出的电量偏大,所以必须增加收集袋,故答案为偏高;
③要将银电量计与电解精炼铜的电解池串联,才能做到通过的电量相同,电解精炼铜时,阳极为粗铜、阴极为精铜,将该银电量计中的银棒与待测电解池的精铜电极相连,铂坩埚接到电源的负极,故答案为:精铜;
(2)①当开关K1闭合,则构成原电池,在中性环境下,金属发生的是吸氧腐蚀,铁棒上发生的反应为Fe-2e=Fe2+,故答案为:Fe-2e=Fe2+;
②当开关K2闭合,则构成电解池,铁是阴极,不被腐蚀,该方法是外加电流的阴极保护法,故答案为:外加电流的阴极。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】元素X、Y、Z位于相同短周期,它们的最高及最低化合价如表所示,下列判断错误的是
元素 | X | Y | Z |
最高、最低化合价 | +7 -1 | +6 -2 | +5 -3 |
A. 原子序数:X>Y>Z
B. 原子半径:X>Y>Z
C. 稳定性:HX>H2Y>ZH3
D. 酸性由强到弱:HXO4>H2YO4>H3ZO4