题目内容
化合物A为一种盐,元素分析表明,A中部分元素的质量分数为:Cu39.50%、N8.64%,其余为H、O、S。A与NaOH混合时有能使湿润的红色石蕊试纸变蓝的气体产生,则A的化学式为
| A.CuNH4SO3 | B.Cu(NH4)2(SO4)2 | C.Cu3(NH4)2(SO4)3 | D.Cu(NH4)2(S2O3)2 |
A
略

练习册系列答案
相关题目

 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。
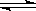 H2(g) + CO(g) △H =" +131.3" kJ/mol
H2(g) + CO(g) △H =" +131.3" kJ/mol