题目内容
【题目】化合物甲只含C、H两种元素,化合物乙和丙都只含C、H、F三种元素,甲、乙、丙都是饱和化合物且分子中都含有26个电子。据此推断:
(1)甲的分子式是________;若甲分子中有两个H原子被F原子代替,所得产物可能有________种结构。
(2)乙是性能优异的环保产品,它可替代某些会破坏臭氧层的氟里昂产品,用作制冷剂。已知乙分子中C、H、F原子个数比为1:2:2,则乙的电子式是________;下列对于乙的描述正确的是________。
A.其分子构型为正四面体 B.其分子构型为正四边形
C.具有两种同分异构体 D.没有同分异构体
(3)将甲、乙按物质的量之比1:1混合所得混合物的平均摩尔质量等于丙的摩尔质量,则丙的分子式是________。
【答案】C3H8 4 ![]() d C2H5F
d C2H5F
【解析】
(1)化合物甲只含C、H两种元素,应为烷烃,分子式符合CnH2n+2,据此结合题意作答;根据二氟代物的可能性采用“定一动一”方法分类讨论。
(2)根据乙分子的构成,结合电子数分析得出分子式;联系甲烷的空间结构判断CH2F2的结构特点;
(3)根据题意求出丙的相对分子质量结合电子数分析作答。
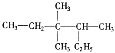
(1) 化合物甲只含C、H两种元素,应为烷烃,分子式符合CnH2n+2,分子中含有26个电子,则有6n+2n+2=26,n=3,则甲为C3H8;若甲分子中有两个H原子被F原子代替,所得产物可能有CH3CH2CHF2、CH3CF2CH3、CH2FCHFCH3、CH2FCH2CH2F共4种,
故答案为:C3H8;4;
(2)乙分子中C.H、F原子个数比为l:2:2,分子中含有26个电子,其分子式应为CH2F2, CH2F2为共价化合物,其电子式为:![]() ,为四面体结构,不是正四面体结构,且不存在同分异构体,故a、b、c项错误,d项正确,
,为四面体结构,不是正四面体结构,且不存在同分异构体,故a、b、c项错误,d项正确,
故答案为:![]() ;d;
;d;
(3)将甲、乙按物质的量之比1:1混合所得混合物的平均摩尔质量等于丙的摩尔质量,则丙的相对分子质量为:![]() =48,且分子中含有26个电子,应为C2H5F,
=48,且分子中含有26个电子,应为C2H5F,
故答案为:C2H5F。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案