题目内容
10.下列各组稀溶液:①氨水和硝酸银 ②氯化铝和氢氧化钠 ③硫酸氢铵和氢氧化钡 ④硝酸和碳酸钠.只用试管、滴管及闻气味就能鉴别的是( )| A. | ③④ | B. | ①②④ | C. | ①②③④ | D. | ②④ |
分析 ①氨水和硝酸银中,反应与氨水的量有关;
②氯化铝和氢氧化钠中,反应与NaOH的量有关;
③硫酸氢铵和氢氧化钡中,反应与氢氧化钡的量有关;
④硝酸和碳酸钠中,反应与硝酸的量有关.
解答 解:①氨水和硝酸银中,氨水不足生成白色沉淀,氨水过量沉淀溶解,则利用试管、滴管相互滴加观察现象可鉴别,故正确;
②氯化铝和氢氧化钠中,NaOH不足生成白色沉淀,NaOH过量沉淀溶解,则利用试管、滴管相互滴加观察现象可鉴别,故正确;
③硫酸氢铵和氢氧化钡中,氢氧化钡不足生成白色沉淀,氢氧化钡过量生成白色沉淀且有刺激性气体生成,则利用试管、滴管及闻气味可鉴别,故正确;
④硝酸和碳酸钠中,硝酸不足无现象,硝酸过量生成无色气体,则利用试管、滴管相互滴加观察现象可鉴别,故正确;
故选C.
点评 本题考查物质的鉴别,为高频考点,把握元素化合物知识及与量有关的反应为解答的关键,注意与量有关的反应中现象的差异为鉴别的依据,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.1mol•L-1的NaCl溶液表示( )
| A. | 溶液中含有1 mol NaCl | B. | 1 mol NaCl溶于1 L水中 | ||
| C. | 58.5 g NaCl溶于941.5 g水中 | D. | 1 L溶液中含有NaCl 58.5 g |
1.下列离子方程式书写正确的是( )
| A. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O═4OH-+2I2 | |
| C. | 向Na2SO3溶液中滴加稀硝酸:SO32-+2H+═SO2↑+H2O | |
| D. | 用氨水吸收足量的CO2气体:OH-+CO2═HCO3- |
18.能正确表示下列反应的离子方程式是( )
| A. | FeO与稀硝酸反应:FeO+2H+═Fe2++H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 溴化亚铁溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2 Br2+6Cl- | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
2.下列物质中不能用于萃取溴水中溴的是( )
| A. | 直馏汽油 | B. | 裂化汽油 | C. | 苯 | D. | 己烷 |
20.海水中蕴藏着丰富的资源.海水综合利用的流程图如图.
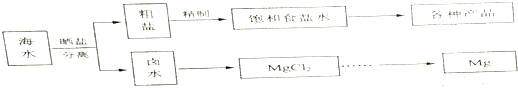
(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
②实验室用惰性电极电解100mL0.1mol/LNaCl溶液,若阴阳两极均得到112mL所体(标准状况),则所得溶液的pH为13(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑.
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品.
①粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去.Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表).若只加一种上述(1)中得到的产品,该物质的化学式为NaClO,控制溶液的pH为9.6≤PH<9.8.
②在家用电热水器不锈钢内胆表面镶嵌镁棒,利用电化学原理来防止内胆腐蚀,写出正极的电极反应式:O2+4e-+2H2O═4OH-.

(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
②实验室用惰性电极电解100mL0.1mol/LNaCl溶液,若阴阳两极均得到112mL所体(标准状况),则所得溶液的pH为13(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑.
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品.
①粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去.Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表).若只加一种上述(1)中得到的产品,该物质的化学式为NaClO,控制溶液的pH为9.6≤PH<9.8.
②在家用电热水器不锈钢内胆表面镶嵌镁棒,利用电化学原理来防止内胆腐蚀,写出正极的电极反应式:O2+4e-+2H2O═4OH-.
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.6 |
| Mg(OH)2 | 9.8 | 11.1 |
 .
.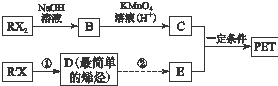 PET是聚酯类合成材料,以卤代烃为原料合成PET的线路如图(反应中部分无机反应物及产物已省略).已知RX2(R、R′代表烃基,X代表卤素原子)是芳香族化合物,相对分子质量为175,其中X元素的质量分数为40.6%.
PET是聚酯类合成材料,以卤代烃为原料合成PET的线路如图(反应中部分无机反应物及产物已省略).已知RX2(R、R′代表烃基,X代表卤素原子)是芳香族化合物,相对分子质量为175,其中X元素的质量分数为40.6%. .
.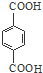 +nHOCH2CH2OH$\stackrel{一定条件下}{→}$
+nHOCH2CH2OH$\stackrel{一定条件下}{→}$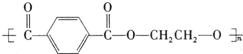 +2nH2O.
+2nH2O.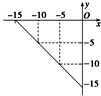 某温度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L.
某温度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L.