��Ŀ����
����Ŀ��A��B��C��D��E��F��G��Ϊ������Ԫ�أ�ԭ���������ε�����AԪ��ԭ�Ӻ��������ӣ�BԪ��ԭ�������������Ǵ�����������2����D�ǵؿ��к�������Ԫ�أ�E�Ƕ������н�������ǿ��Ԫ�أ�F��Gλ�����ڣ�G��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���ش��������⣨��ӦԪ�ؾ���Ԫ�ط��ű�ʾ����
��1��C��Ԫ�����ڱ��е�λ��Ϊ �� G��ԭ�ӽṹʾ��ͼ�� ��
��2��D��E��ԭ�Ӹ�����1��1�γɻ�����ף������ʽΪ �� ������ѧ������Ϊ ��
��3������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�� ��
��4��E��F��G����Ԫ�����γɵļ����ӣ��뾶�ɴ�С��˳���� ��
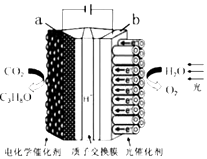
��5����BA4��D2��EDA��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��BA4���壬b��ͨ��D2���壬��a���Ǹõ�ص����������ĵ缫��ӦʽΪ ��
���𰸡�
��1���ڶ����ڵ�VA�壻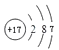
��2��![]() �����Ӽ������ۼ�
�����Ӽ������ۼ�
��3��2Na2O2+2H2O�T4NaOH+O2��
��4��S2����Cl����Na+
��5��������O2+2H2O+4e���T4OH��
���������⣺A��B��C��D��E��F��G��Ϊ������Ԫ�أ�ԭ���������ε�����AԪ��ԭ�Ӻ��������ӣ���AΪ��Ԫ�أ�BԪ��ԭ�Ӻ��������������Ǵ�����������2������B��2�����Ӳ㣬�������4�����ӣ���BΪ̼Ԫ�أ�DԪ���ǵؿ��к�������Ԫ�أ���DΪ��Ԫ�أ�Cԭ����������̼����֮�䣬��CΪ��Ԫ�أ�EԪ���Ƕ�����Ԫ���н�������ǿ��Ԫ�أ���EΪNa��F��G��λ�����ڣ�G��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�����֪FΪSԪ�ء�GΪClԪ�أ���1��C�ǵ�Ԫ�أ�ԭ����2�����Ӳ㣬����������Ϊ5����Ԫ�����ڱ��е�λ�ã��ڶ����ڵ�VA�壬GΪClԪ�أ�ԭ�ӽṹʾ��ͼ��  �����Դ��ǣ��ڶ����ڵ�VA�壻
�����Դ��ǣ��ڶ����ڵ�VA�壻  ����2��D��E��ԭ�Ӹ�����1��1�γɻ������ΪNa2O2 �� �����ʽΪ
����2��D��E��ԭ�Ӹ�����1��1�γɻ������ΪNa2O2 �� �����ʽΪ ![]() ��������ѧ������Ϊ�����Ӽ������ۼ������Դ��ǣ�
��������ѧ������Ϊ�����Ӽ������ۼ������Դ��ǣ� ![]() �����Ӽ������ۼ�����3������������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2H2O�T4NaOH+O2�������Դ��ǣ�2Na2O2+2H2O�T4NaOH+O2������4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶�ɴ�С��˳���ǣ�S2����Cl����Na+ �� ���Դ��ǣ�S2����Cl����Na+����5����CH4��O2��NaOH��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��CH4���壬b��ͨ��O2���壬���鷢��������Ӧ����a���Ǹõ�صĸ�����bΪ������������������õ��ӣ������������������������ӣ������ĵ缫��ӦʽΪ��O2+2H2O+4e���T4OH�� �� ���Դ��ǣ�����O2+2H2O+4e���T4OH�� ��
�����Ӽ������ۼ�����3������������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2H2O�T4NaOH+O2�������Դ��ǣ�2Na2O2+2H2O�T4NaOH+O2������4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶�ɴ�С��˳���ǣ�S2����Cl����Na+ �� ���Դ��ǣ�S2����Cl����Na+����5����CH4��O2��NaOH��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��CH4���壬b��ͨ��O2���壬���鷢��������Ӧ����a���Ǹõ�صĸ�����bΪ������������������õ��ӣ������������������������ӣ������ĵ缫��ӦʽΪ��O2+2H2O+4e���T4OH�� �� ���Դ��ǣ�����O2+2H2O+4e���T4OH�� ��