题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 将少量Fe(NO3)2试样加水溶解,滴加稀H2SO4酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2试样已变质 |
| B | 将少量某无色气体通入澄清石灰水 | 出现白色沉淀 | 该气体一定是CO2 |
| C | 分别测定常温下0.1 mol·L-1 Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3> Na2CO3 | 非金属性:Si>C |
| D | 向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中,滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D
向Fe(NO3)2中滴加稀H2SO4后,溶液中存在H+和NO3-,具有强氧化性,可以将Fe2+氧化为Fe3+,滴加KSCN溶液必然变为红色,A项错误;SO2气体通入澄清石灰水中发生反应:Ca(OH)2+SO2=CaSO3↓+H2O,也会出现白色沉淀,B项错误;Na2SiO3和Na2CO3均为强碱弱酸盐,水解显碱性,碱性越强,则对应的酸的酸性越弱,可知酸性H2SiO3<H2CO3,非金属性Si<C, C项错误;当溶液中可以产生两种难溶物的时候,溶度积小的先生成,D项正确。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
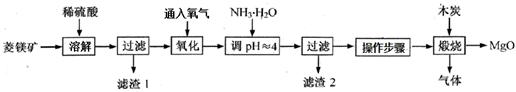
 2MgO+2SO2↑+CO2↑; MgSO4+C
2MgO+2SO2↑+CO2↑; MgSO4+C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
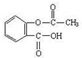 ),是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为:
),是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为: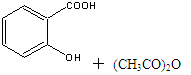

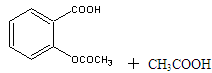


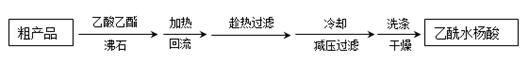
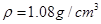 ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 (百分数精确到0.1)。
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 (百分数精确到0.1)。