题目内容
在Na2SO4和Al2(SO4)3的混合溶液中,如果[SO42-]=0.3mol?L-1,当加入等体积的0.2 mol/L的NaOH溶液时,生成沉淀恰好完全溶解,则原混合溶液中Na+物质的量浓度是:
| A.0.5 mol/L | B.0.3 mol/L | C.0.45 mol/L | D.0.225 mol/L |
C
由题意知反应的方程式为Al2(SO4)3+8NaOH=2NaAlO2+3Na2SO4+4H2O,因此硫酸铝的浓度为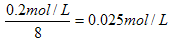 ,即;硫酸铝中c(SO32-)=0.075mol·L-1。所以硫酸钠的浓度是0.3mol/L-0.075mol/L=0.225mol/L,所以钠离子浓度0.225mol/L×2=0.45mol/L。因此答案选C。
,即;硫酸铝中c(SO32-)=0.075mol·L-1。所以硫酸钠的浓度是0.3mol/L-0.075mol/L=0.225mol/L,所以钠离子浓度0.225mol/L×2=0.45mol/L。因此答案选C。
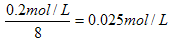 ,即;硫酸铝中c(SO32-)=0.075mol·L-1。所以硫酸钠的浓度是0.3mol/L-0.075mol/L=0.225mol/L,所以钠离子浓度0.225mol/L×2=0.45mol/L。因此答案选C。
,即;硫酸铝中c(SO32-)=0.075mol·L-1。所以硫酸钠的浓度是0.3mol/L-0.075mol/L=0.225mol/L,所以钠离子浓度0.225mol/L×2=0.45mol/L。因此答案选C。
练习册系列答案
相关题目