题目内容
把0.02 mol/L CH3COOH溶液和0.01 mol/L NaOH溶液以等体积混和后溶液显酸性,则混合液中微粒浓度关系正确的为
| A.c(CH3COO-)<c(Na+) |
| B.c(CH3COOH)+c(CH3COO-)="0.02" mol/L |
| C.c(CH3COOH)>c(CH3COO-) |
| D.c(OH-)+c(CH3COO-)=c(H+)+c(Na+) |
D
解析试题分析:将0.02 mol·L-1 CH3COOH和0.01 mol·L-1NaOH等体积混合后,混合液的溶质为CH3COOH和CH3COONa,且等物质的量浓度,都是0.005 mol·L-1。由于CH3COOH的电离趋势大于CH3COO-的水解趋势,所以,c(CH3COO-)>c(Na+);且c(CH3COOH)<c(CH3COO-) ,所以AC错误;但无论怎么变化,由物料守恒知:c(CH3COOH)+c(CH3COO-)=0.01 mol·L-1。B错误;D.c(OH-)+c(CH3COO-)=c(H+)+c(Na+),电荷守恒的式子,正确。
考点:溶液中微粒之间的关系

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验:①0.1mol·L-1AgNO3溶液和0.1mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到
滤液b和白色沉淀c;②向滤液b中滴加0.1mol·L-1KI溶液,出现浑浊;③向沉淀c中滴加0.1mol·L-1KI溶液,沉淀变为黄色。下列分析不正确的是:
A.浊液a中存在沉淀溶解平衡:AgCl(g) 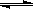 Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
| B.滤液b中不含有Ag+ |
| C.③中颜色变化说明AgCl转化为AgI |
| D.实验可以证明AgI比AgCl更难溶 |
将标准状况下1.12L氨气溶于500mL水中配制成溶液,从中取出5mL,有关这5mL溶液的叙 述正确的是
| A.溶液中c(NH4+)< c(OH—) | B.氨水的物质的量浓度为0.1 mol·L—1 |
| C.溶液的pH>13 | D.与5mL 0.1mol·L—1HCl溶液恰好完全中和 |
在H2O+CH3COO- CH3COOH+OH-的平衡中,要使平衡向右移动,应采取的措施是
CH3COOH+OH-的平衡中,要使平衡向右移动,应采取的措施是
| A.加入NaOH固体 | B.加入冰醋酸 | C.增大压强 | D.升高温度 |
下列叙述正确的是
| A.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:2c(Na+) + c(CH3COOH) = c(CH3COO-) +2c(OH-) |
| B.Ksp(AgCl)>Ksp(AgI)由此可以判断AgCl(S) + I- = AgI(S) + Cl-能够发生 |
| C.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| D.中和浓度与体积均相等的盐酸和醋酸溶液,消耗NaOH的物质的量不相等 |
下列事实中不能证明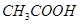 是弱电解质的是
是弱电解质的是
A.常温下某 |
B.常温下0.1mol 溶液的pH=2.8 溶液的pH=2.8 |
C. 溶液与稀盐酸反应生成 溶液与稀盐酸反应生成 |
D.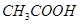 属于共价化合物 属于共价化合物 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:c(Na+)>c(Cl-) |
| C.已知Ka(HF)=7.2×10-4,Ka(HCN)=6.2×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 |
| D.浓度均为0.1 mol·L-1的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:③>②>① |