题目内容
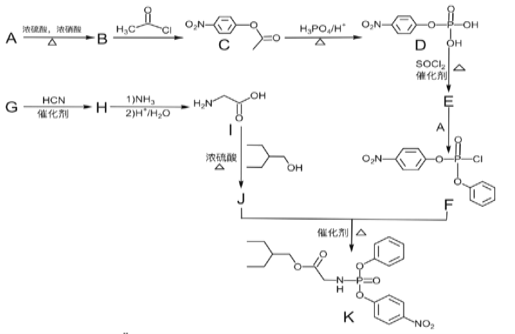
【题目】据研究报道,药物瑞德西韦(Remdesivir)对2019年新型冠状病毒(COVID—19)有明显抑制作用。K为药物合成的中间体,其合成路线如图:
已知:(1)R—OH![]() R—Cl
R—Cl
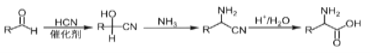
(2)
回答下列问题:
(1)B的化学名称为__。
(2)J中含氧官能团的名称为__。
(3)B到C的反应类型是___,G到H的反应类型是__。
(4)由G生成H的化学反应方程式为___。
(5)E中含两个Cl原子,则E的结构简式___。
(6)X是C同分异构体,写出满足下列条件的X的结构简式___。
①苯环上含有硝基且苯环上只有一种氢原子;②遇FeCl3溶液发生显色反应;③1mol的X与足量金属Na反应可生成2gH2。
(7)参照F的合成路线图,设计由![]() 、SOCl2为原料制备
、SOCl2为原料制备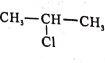 的合成路线(无机试剂任选)___。
的合成路线(无机试剂任选)___。
【答案】对硝基苯酚(4—硝基苯酚) 酯基 取代反应 加成反应 HCHO+HCN![]()
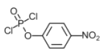
 、
、
【解析】
A发生取代反应生成B,B发生取代反应生成C,根据C结构简式知,B为![]() ,则A为
,则A为![]() ,D发生信息1的反应生成E,E中含两个Cl原子,则E为
,D发生信息1的反应生成E,E中含两个Cl原子,则E为 ,E和A发生取代反应生成F,G发生信息2的反应生成H,H发生取代反应、水解反应得到I,根据I结构简式知H为HOCH2CN,G为HCHO,I发生酯化反应生成J,F与J发生取代反应生成K,J为
,E和A发生取代反应生成F,G发生信息2的反应生成H,H发生取代反应、水解反应得到I,根据I结构简式知H为HOCH2CN,G为HCHO,I发生酯化反应生成J,F与J发生取代反应生成K,J为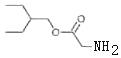 ,据此解答。
,据此解答。
(1)B为![]() ,B的化学名称为对硝基苯酚或4硝基苯酚;故答案为:对硝基苯酚或4硝基苯酚;
,B的化学名称为对硝基苯酚或4硝基苯酚;故答案为:对硝基苯酚或4硝基苯酚;
(2)J为 ,J中含氧官能团的名称为酯基;故答案为:酯基;
,J中含氧官能团的名称为酯基;故答案为:酯基;
(3)B为![]() ,B中氢原子被CH3CO取代生成C,B到C的反应类型取代反应;G为HCHO,H为HOCH2CN,G中碳氧双键与HCN发生加成反应得H,故答案为:取代反应;加成反应;
,B中氢原子被CH3CO取代生成C,B到C的反应类型取代反应;G为HCHO,H为HOCH2CN,G中碳氧双键与HCN发生加成反应得H,故答案为:取代反应;加成反应;
(4)H为HOCH2CN,G为HCHO,由G生成H的化学反应方程式为HCHO+HCN![]()
![]() (或
(或![]() + HCN
+ HCN![]()
![]() );故答案为:HCHO+HCN
);故答案为:HCHO+HCN![]()
![]() (或
(或![]() + HCN
+ HCN![]()
![]() );
);
(5)根据分析,E为 ;故答案为:
;故答案为: ;
;
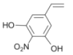
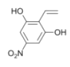
(6)C是对硝基乙酸苯酯,X是C同分异构体,X的结构简式满足下列条件:①苯环上含有硝基且苯环上只有一种氢原子;②遇FeCl3溶液发生显色反应,说明含有酚羟基;③1mol的X与足量金属Na反应可生成2gH2,生成1mol氢气,则含有两个羟基,根据不饱和度知还存在CH=CH2,该分子结构对称,符合条件的结构简式为 ;故答案为:
;故答案为: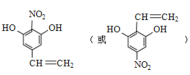 ;
;
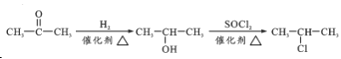
(7)由![]() 、SOCl2为原料制备
、SOCl2为原料制备 ,可先将
,可先将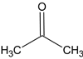 还原成
还原成 ,根据已知(1)R—OH
,根据已知(1)R—OH![]() R—Cl,在SOCl2、催化剂、加热条件下得到
R—Cl,在SOCl2、催化剂、加热条件下得到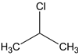 ,合成路线为:
,合成路线为: ,故答案为:
,故答案为: 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案