题目内容
19.如图是几种常见有机物之间的转化关系,有关说法正确的是( )
| A. | a只能是淀粉 | |
| B. | 反应①②③均为取代反应 | |
| C. | 乙醇可以与多种氧化剂发生氧化反应 | |
| D. | 乙酸乙酯的羧酸类同分异构体只有1种 |
分析 由图中转化关系可知,a为淀粉或纤维素,①为水解反应生成葡萄糖,②为葡萄糖的酒化反应生成乙醇,③为乙醇的酯化反应生成乙酸乙酯,结合有机物的性质来解答.
解答 解:A.由上述分析可知,a为淀粉或纤维素,故A错误;
B.①③为取代反应,②为分解反应,故B错误;
C.乙醇可发生催化氧化、燃烧反应,且能被强氧化剂氧化,故C正确;
D.乙酸乙酯的羧酸类同分异构体含-COOH,-C3H7有2种,羧酸类同分异构体只有2种,故D错误;
故选C.
点评 本题考查有机物的推断,为高频考点,把握图中转化、有机物的性质为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到烧杯中的FeCl2溶液中
②过量氨水溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中滴入少量NaHSO4溶液
⑤向饱和Na2CO3溶液中通入足量CO2 .
①金属钠投入到烧杯中的FeCl2溶液中
②过量氨水溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中滴入少量NaHSO4溶液
⑤向饱和Na2CO3溶液中通入足量CO2 .
| A. | ①③④⑤ | B. | 只有①④ | C. | 只有③④⑤ | D. | 只有②③④⑤ |
10.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 25°时,在pH=0的溶液中,NO3-、SO42-、I-、K+ | |
| B. | 0.1mol/L的Fe(NO3)3溶液中:Na+、H+、Cl-、SCN- | |
| C. | 0.1mol/L的NaAlO2溶液中:K+、Al3+、NO3-、SO42- | |
| D. | 由水电离产生的c(H+)=1×10-13mol/L的溶液中:Na+、Ba2+、NO3-、Cl- |
7.下列关于化学与生产、生活的分析不正确的是( )
| A. | 酸雨是碳氮硫的氧化物大量排放引起的 | |
| B. | “火树银花”焰火的实质是金属元素的焰色反应 | |
| C. | 侯氏制碱法所用氨水是利用了其碱性 | |
| D. | 工业上由石油获取乙烯过程中既有物理变化又有化学变化 |
14. A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的$\frac{1}{4}$,C元素的最高价氧化物的水化物是一种中强碱.甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )
A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的$\frac{1}{4}$,C元素的最高价氧化物的水化物是一种中强碱.甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )
 A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的$\frac{1}{4}$,C元素的最高价氧化物的水化物是一种中强碱.甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )
A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的$\frac{1}{4}$,C元素的最高价氧化物的水化物是一种中强碱.甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )| A. | C、D两元素形成化合物属共价化合物 | |
| B. | A、D分别与B元素形成的化合物都是大气污染物 | |
| C. | C、D的简单离子均能促进水的电离 | |
| D. | E的氧化物水化物的酸性大于D的氧化物水化物的酸性 |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应转移电子数一定为3NA | |
| B. | 标准状况下,2.24LNH3中含有共价键的数目为NA | |
| C. | 标况下,11.2LSO3所含的分子数目为0.5NA | |
| D. | lmolNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
11.下列设计的实验方案能达到相应实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 蛋白质发生了变性 | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液 |
| B | 证明反应速率会随反应物浓度的增大而加快 | 用3mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然 后加入1mL 1mol•L-1CuSO4溶液,迅速产生较多气泡 |
| C | 比较Ksp(BaCO3)、Ksp(BaSO4) | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤, 向洗净的沉淀中加稀盐酸,有气泡产生 |
| D | 通过观察液面差判断该装置的气密性 | 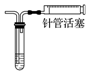 向里推注射器 向里推注射器 |
| A. | A | B. | B | C. | C | D. | D |
8.常温下,往某浓度的氯水中滴人Na2SO3溶液的pH变化如图所示,下列离子浓度的关系错误的是( )

| A. | a点:c(H+)>c(Cl-)>c(ClO-) | |
| B. | b点:$\frac{1}{2}$ c(Cl-)═c(SO42-)=0.005mol•L-1 | |
| C. | c点:c(Na+)═2c(HSO3-)+2c(SO32-) | |
| D. | d 点:c(Na+)═c(Cl-)+c(HSO3-)+2c(SO32-)+2c(SO42-) |
13.H2S为二元弱酸.20℃时,向0.100mol/L的Na2S溶液中缓慢通入HCl气体(忽略溶液体积的变化及H2S的挥发).下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
| A. | 通入HCl气体之前:c(S2-)>c(HS-)>c(OH-)>c(H+) | |
| B. | pH=7的溶液中:c(Cl-)>c(HS-)+2c(H2S) | |
| C. | c(HS-)=c(S2-)的碱性溶液中:c(Cl-)+c(HS-)>0.100 mol•L-1+c(H2S) | |
| D. | c(Cl-)=0.100 mol•L-1的溶液中:c(OH-)-c(H+)=c(H2S)-c(S2-) |